Caratteristiche generali della Malattia celiaca
La Celiachia o malattia celiaca è un’enteropatia dovuta ad intolleranza al glutine, contenuto in alcuni cereali assunti con la dieta (frumento, segale, orzo, farro e avena). Essa si presenta in soggetti geneticamente predisposti in seguito all’assunzione di glutine ed in presenza di fattori scatenanti. Tali fattori non sono del tutto noti, e comprendono lo stress ed alcune infezioni virali intestinali.
Sintomatologia della Malattia celiaca
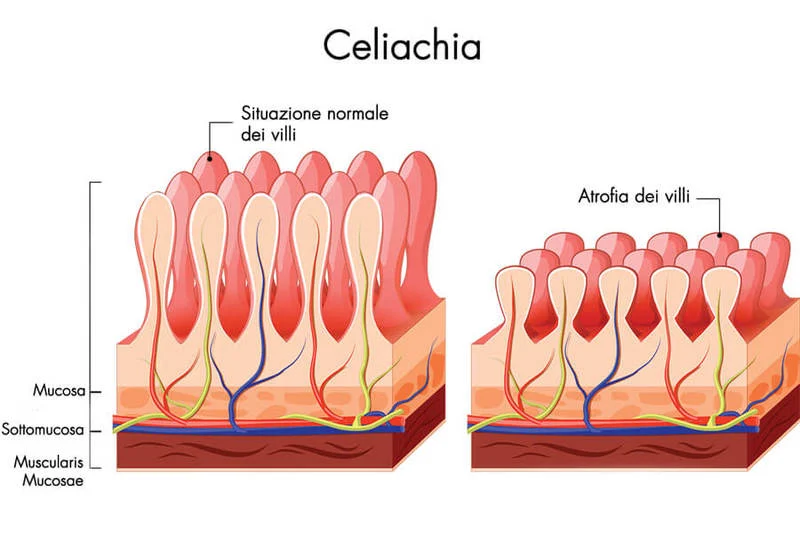
La malattia è caratterizzata da danno alla mucosa dell’intestino tenue e malassorbimento. Inizialmente la celiachia era considerata una malattia dell’infanzia, che si sviluppava dopo lo svezzamento, nei primi 6-24 mesi di vita, e caratterizzata da diarrea cronica, scarsa crescita e gonfiore addominale (forma classica).
In realtà la malattia può presentarsi ad ogni età, e nell’adulto possono prevalere dei sintomi extraintestinali, a dare la cosiddetta forma atipica, caratterizzata da anemia, osteoporosi, alopecia, infertilità, dolori addominali. Esistono anche delle forme relativamente asintomatiche, che sono spesso scoperte mediante screening di soggetti a rischio.
Sono note in particolare una forma silente, asintomatica nonostante il danno intestinale, ed una forma latente in cui sono presenti gli autoanticorpi tipici della malattia in assenza di lesioni alla mucosa intestinale.
Componente genetica di suscettibilità
La celiachia presenta una forte componente genetica multifattoriale come dimostrato dagli studi familiari. E’ stata osservata infatti una concordanza del 75% tra gemelli monozigoti, ed un aumento del rischio di sviluppare la malattia nei fratelli degli affetti di circa dieci volte rispetto alla popolazione generale. Il fatto che non vi sia concordanza del 100% tra i gemelli monozigoti implica la presenza di altri fattori (ambientali) oltre a quelli genetici per lo svilupparsi della malattia.
Il ruolo degli alleli HLA
Il fattore genetico predominante nella predisposizione alla malattia celiaca è dato da alcuni alleli MHC (complesso maggiore di istocompatibilità) di classe seconda che mappano nel locus HLA-DQ sul cromosoma 6 (6p21). In particolare, è stato osservato che il 90-95% dei soggetti celiaci sono portatori degli alleli che codificano per la molecola HLA-DQ2. Questo è un eterodimero che è composto dalla catena alfa codificata da un allele del gruppo allelico HLA-DQA1*05 e da una catena beta codificata da un allele del gruppo allelico HLA-DQB1*02.
HLA-DQ2
Gli alleli HLA codificanti l’eterodimero HLA-DQ2 possono essere ereditati in cis, cioè essere presenti su uno solo dei cromosomi parentali, nell’aplotipo DR3-DQ2. Oppure possono essere ereditati in trans, con uno degli alleli presenti su ognuno dei due cromosomi parentali, nell’eterozigote per gli aplotipi DR5-DQ7/DR7-DQ2. La quasi totalità dei soggetti celiaci negativi per HLA-DQ2 sono portatori degli alleli che codificano per la molecola HLA-DQ8. Questo è un eterodimero composto da una catena alfa codificata da un allele del gruppo allelico HLA-DQA1*03 e da una catena beta codificata dall’allele HLA-DQB1*03:02.
I pochi soggetti celiaci che sono negativi sia per HLA-DQ2 che per HLA-DQ8 sono spesso portatori di solo mezzo eterodimero, di solito codificato da un allele del gruppo allelico HLA-DQB1*02. E’ stato inoltre osservato che l’omozigosi per HLA-DQB1*02 era associata ad una malattia più severa. Gli alleli HLA rendono conto di circa il 40% della suscettibilità genetica alla malattia celiaca. Il resto del contributo genetico sarebbe dato da numerosi altri geni ciascuno dei quali con un piccolo effetto.
Tra la popolazione caucasica circa il 30% dei soggetti è portatore dell’eterodimero HLA-DQ2. L’incidenza della malattia è stata stimata di circa 1/100 – 1/150 in Europa e Nord America. Ciò implica la presenza di fattori ambientali che scatenano la patologia in presenza di alleli HLA predisponenti e di ingestione di glutine. Tali fattori sono noti solo in parte, e comprendono lo stress ed infezioni virali intestinali.
Meccanismo patogenetico
Il fattore genetico predisponente principale è dato dalla presenza di geni HLA che codificano per gli eterodimeri HLA-DQ2 e HLA-DQ8. Si tratta di molecole presenti sulle cellule APC (Antigen Presenting Cell – cellule presentanti l’antigene) del sistema immunitario. Sono cellule che inglobano, processano e presentano gli antigeni sulla loro superficie legandoli agli eterodimeri di molecole HLA.
In tal modo i linfociti T sono in grado di riconoscere le molecole estranee e di innescare una risposta immunitaria. Gli eterodimeri HLA-DQ2 ed HLA-DQ8 sono in grado di legare le molecole di glutine sulla superficie delle APC e di presentarle ai linfociti T presenti nella lamina propria dell’intestino tenue.
Il glutine
Il glutine è dato dalla frazione alcol-solubile delle proteine presenti nei cereali, in particolare gliadine e glutenine. Queste proteine hanno un alto contenuto amminoacidico in prolina e glutammina. Gli eterodimeri HLA-DQ2 e HLA-DQ8 hanno una composizione amminoacidica tale, nella loro tasca di legame per l’antigene, da avere un’alta affinità per accogliere peptidi carichi negativamente, è ciò ha reso a lungo inspiegabile il fatto che legassero peptidi derivati dal glutine che è ricco in glutammina, un aminoacido neutro. L’enigma è stato spiegato quando si è scoperto che i soggetti celiaci producevano anticorpi anti transglutamminasi tissutale.
Il ruolo della transglutamminasi tissutale
La transglutamminasi tissutale è rilasciata nella mucosa intestinale in presenza di danno tissutale in quanto coinvolta nella riparazione. E’ stato osservato che la transglutamminasi tissutale possiede una grande avidità per i peptidi di glutine, e che in certe condizioni, come un pH basso, può deamminare la glutammina. In questo modo i residui di glutammina, neutri, sono convertiti in acido glutammico, un amminoacido carico negativamente. Così, alcuni peptidi derivati dal glutine e deamminati, grazie alla carica negativa dell’acido glutammico, mostrano un’aumentata affinità di legame con gli eterodimeri HLA-DQ2 e HLA-DQ8.
In questo modo i linfociti T HLA-DQ2 e HLA-DQ8 ristretti sono attivati, in una risposta di tipo Th1, ed in questo modo inducono la produzione di anticorpi e di citochine, tra cui l’interferon-gamma (IFN-gamma) che determinano il danno alla mucosa intestinale. E’ stato ipotizzato che alcune situazioni ambientali che causano potenzialmente un danno intestinale, come l’infezione con virus intestinali, possano creare un ambiente favorevole all’insorgenza della celiachia in quanto possono indurre un ambiente proinfiammatorio che induce la produzione di IFN-gamma e l’attivazione delle cellule APC, inducendole ad aumentare l’espressione di eterodimeri HLA.
Ciò può essere accompagnato da danno alla mucosa intestinale con rilascio di transglutamminasi tissutale. In questo scenario ipotetico, i virus o altri patogeni intestinali creano un ambiente ideale per l’attivazione delle risposte immunitarie HLA-DQ2 e HLA-DQ8 ristrette quando il glutine venga ad essere presente nel lume intestinale. La produzione di citochine, quindi amplifica il danno alla mucosa portando alla perdita della struttura dei villi intestinali ed ipertrofia delle cripte.
Diagnostica e terapia
La diagnosi di celiachia si effettua mediante la sierologia e la biopsia intestinale. Gli esami vanno effettuati quando il paziente segue una dieta libera (contenente glutine) per evitare falsi negativi. Il primo test diagnostico introdotto negli anni ’80 era quello degli anticorpi antigliadina (AGA) di classe IgA e IgG, che hanno però una bassa sensibilità e specificità, che ne limita l’uso al monitoraggio della patologia e della compliance della dieta da parte del paziente.
La ricerca degli EMA
Gli anticorpi antiendomisio (EMA) sono autoanticorpi di classe IgA o IgG diretti contro le proteine della matrice extracellulare. La ricerca degli EMA viene utilizzata sia per la diagnosi che per il monitoraggio della malattia. Infine, sono stati individuati gli anticorpi anti transglutamminasi tissutale. Possono essere ricercati per la diagnosi sia anticorpi di classe IgG che IgA, fatto molto importante per la diagnosi di soggetti con deficit IgA (circa il 20% dei soggetti celiaci presenta un deficit selettivo di IgA) e perché sono stati riportati casi di soggetti senza deficit IgA che erano positivi solo per IgG.
Biopsia
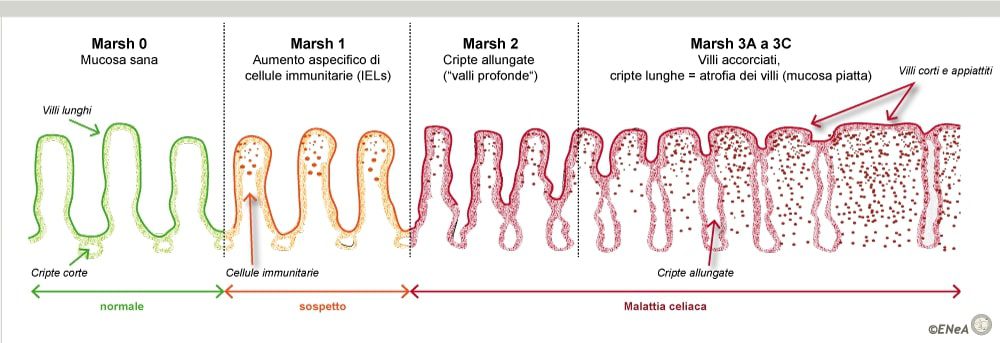
Infine, la biopsia intestinale rimane il gold standard per la diagnosi di celiachia in quanto permette di evidenziare le lesioni alla mucosa intestinale. Nel caso di presenza della malattia all’interno di una famiglia, data la sua caratteristica predisposizione genetica, è opportuno effettuare uno screening degli anticorpi in tutti i parenti di primo grado del malato.
Test di tipizzazione HLA
Il test genetico di tipizzazione HLA per l’individuazione degli alleli di suscettibilità HLA-DQ2 e HLA-DQ8 alla malattia celiaca è da considerarsi un test di secondo livello da eseguirsi nei casi dubbi, quando i saggi anticorpali o la biopsia abbiano dato risultati dubbi o discordanti. Il test ha un alto valore predittivo negativo, in quanto nei soggetti negativi per HLA-DQ2 e DQ8 la probabilità di sviluppare la patologia è estremamente bassa. Pertanto, può essere utile per decidere se continuare il monitoraggio degli anticorpi nei soggetti ad alto rischio (per esempio i parenti di primo grado di un soggetto affetto) che siano risultati negativi ai test sierologici.
Conclusioni
Ad oggi l’unica terapia possibile è una dieta priva di glutine per tutta la vita. La dieta deve essere seguita rigorosamente, evitando le trasgressioni. Va inoltre tenuto sempre presente il rischio di contaminazioni accidentali dei cibi con il glutine, che possono portare ad assunzione involontaria. Per questo motivo, grande attenzione deve essere posta nella manipolazione e cottura dei cibi e nel controllo delle etichette. Per chi soffre di celiachia è sufficiente l’assunzione anche di un quantitativo molto ridotto di un alimento che contiene glutine per provocare un danno alla salute. La dieta priva di glutine consente di eliminare i sintomi e di ricostituire i tessuti intestinali, di solito entro sei-diciotto mesi dalla diagnosi.
Questo articolo vuole essere informativo, e non è sostitutivo di un consulto con il proprio medico per trattare eventuali problemi di salute.
Fonti
- https://it.wikipedia.org/wiki/Celiachia
- https://www.epicentro.iss.it/celiachia/
- Antonozzi I e Gulletta E, Medicina di laboratorio. Logica e patologia clinica. Piccin, 2013
- Kagnoff MF, Celiac disease: pathogenesis of a model immunogenetic disease. The Journal of Clinical investigation; 2007, 117(1):41-49
- Corso ECM FAD AIBT “HLA e malattie autoimmuni: come, quando e perché”, 2010. A cura di Martinetti M e Mascaretti L.
- https://www.microbiologiaitalia.it/batteriologia/sensibilita-al-glutine-non-celiaca-la-disbiosi-intestinale-potrebbe-esserne-la-causa/