Caratteristiche
Con il termine “epatite” si fa riferimento ad una infiammazione a carico del fegato, sia essa acuta o cronica, in cui viene alterato lo status fisiologico e lo status istologico dell’organo, con un conseguente processo distruttivo a carico delle cellule epatiche (epatociti) e del tessuto epatico. Le cause di questa patologia possono essere molteplici ed a tal proposito in base all’eziologia vengono differenziate in:
- epatiti di origine virale, in cui rientrano le epatiti causate sia da virus epatotropi, come HAV, HBV, HCV, HDV, HEV e HGV sia da virus non epatospecifici, come il CMV, i Coxsackie virus che possono innescare un processo di epatite secondario.
- epatiti di origine non virale, dove solitamente vengono classificati tutti quei disordini a carico del fegato conseguenti a reazioni autoimmunitarie, reazioni farmacologiche e sostanze chimiche. Anche alcuni disordini metabolici congeniti o acquisiti possono far scaturire un processo infiammatorio epatico.
Un’altra modalità, inoltre, per discriminare le epatiti, è quella di suddividerle in acute e croniche: le epatiti acute, i cui sintomi riguardano nausea, dolore al quadrante superiore destro, astenia e comparsa di ittero, generalmente tendono a risolversi spontaneamente, salvo alcuni casi in cui possono evolvere nella cronicizzazione. L’epatite cronica, invece, può decorrere silente per anni per poi manifestarsi con segnali anche molto gravi (come l’encefalopatia epatica da ammoniemia) quando il quadro clinico è già avanzato (cirrosi epatica scompensata). L’epatite cronica è causata da virus quali HBV ed in particolare HCV, ma anche da epatiti autoimmuni e/o steatoepatiti.
I virus epatospecifici sono responsabili di alterazioni epatiche che nel corso del tempo possono indurre conseguenti alterazioni metaboliche sistemiche. Tra questi, il virus dell’epatite C di cui tratteremo nello specifico, è senza alcun dubbio il più pericoloso e temuto, nonostante sia divenuto curabile con i nuovi farmaci antivirali DAA ma per cui al tempo stesso non è presente un vaccino tale da eradicare a monte la possibilità di infezione. La scoperta del virus HCV, avvenuta alla fine degli anni ’80, è valsa ai virologi Harvey J. Alter, Charles M. Rice e Michael Houghton, il premio Nobel per la medicina 2020.
Eziologia e patogenesi
L’epatite C è una patologia ad eziologia virale, il cui virus responsabile è l‘Hepatitis C Virus, virus a RNA a singolo filamento appartenente alla famiglia dei Flaviviridae. La patogenesi e conseguentemente il progredire del processo morboso avviene per l’abnorme reazione immuno-patologica cellulo-mediata; infatti, il danno che il virus HCV reca al fegato è principalmente immuno-mediato: esso, infatti, prima di giungere al suo organo d’elezione, infetta i linfociti T e B. La velocità di replicazione del virus è molto alta (1×1012 virioni al giorno circa). La risposta immunitaria innata si manifesta inizialmente con la produzione di citochine ma, alcune proteine codificate da HCV come il core, NS3A, NS4A, NS4B permettono al virus di eludere le difese immunitarie innate ed iniziare così una attiva replicazione virale: ciò comporta, nella maggioranza dei casi, la persistenza e la cronicizzazione dell’infezione, con lesioni isto-citopatiche ben evidenti.
Segni e sintomi
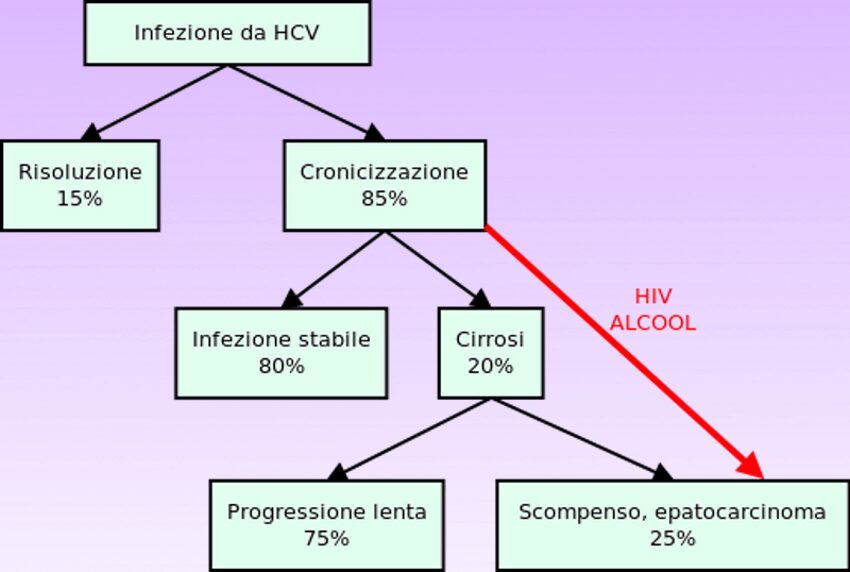
Nella grande maggioranza dei casi, l’instaurarsi della patologia e la sua lenta evoluzione avviene in maniera silente. In alcuni pazienti, la fase acuta, che si ha quando l’organismo subito dopo l’infezione cerca di combattere il virus, può comunque manifestarsi con dei sintomi, quali nausea, dolore alle articolazioni, astenia, presenza di ittero – tipica colorazione giallastra della cute e delle sclere causata da un aumento dei livelli di bilirubina nel sangue (> 2,5 mg/mL). La comparsa di ittero è caratteristica dei disordini epatici. Diversi studi hanno dimostrato che circa l’80 % dei pazienti infettati dal virus sviluppa un’infezione cronica. Quest’ultima è estremamente subdola, poiché per decenni può decorrere senza particolari manifestazioni cliniche, eccetto un senso di affaticamento e stanchezza tipici della patologia. Dopo molti anni e spesso improvvisamente l’epatite C può manifestarsi quando il fegato è già in uno stadio di compromissione avanzata, nel caso della cirrosi epatica e dell’epatocarcinoma.
Complicanze
La cirrosi epatica ed il carcinoma epatocellulare sono le due gravissime complicanze in cui l’infezione cronica da HCV può evolvere. La cirrosi epatica è caratterizzata da un continuo processo fibrotico causato dalla necrosi del parenchima epatico che nel protrarsi del tempo comporta un sovvertimento totale della funzione e della struttura del fegato. La necrosi del parenchima comporta una successiva “riparazione” del tessuto con rigenerazione nodulare per iperplasia a cui segue l’instaurarsi di una fibrosi. Questa totale perdita strutturale si ripercuote sia sulla funzione fisiologica del fegato che non riesce più a svolgere le sue caratteristiche funzioni, sia sulla circolazione portale con sviluppo di ipertensione portale. La cirrosi è considerata quindi la fase “terminale” del fegato nell’epatite C. I sintomi riguardano ascite, ittero, angioma stellare sulla cute, edema degli arti inferiori. Nel caso della cirrosi epatica scompensata, le manifestazioni sono più violente, e riguardano il sanguinamento delle varici esofagee per loro rottura e l’encefalopatia epatica.
L’encefalopatia epatica, il cui stadio avanzato è conosciuto come coma epatico, viene a verificarsi quando il fegato non riesce più ad eliminare le sostanze tossiche per l’organismo, che di conseguenza si accumulano nel sangue. In particolare, i composti che non vengono metabolizzati sono quelli contenenti azoto, poiché il ciclo dell’urea appare notevolmente ridotto essendo il fegato in un deficit funzionale. Il composto causa principale di encefalopatia è l’ammonio (ammoniemia) che riesce ad oltrepassare la barriera ematoencefalica causando così diversi sintomi neurologici, come letargia, confusione mentale, alterazione dei livelli di coscienza, alterazione dello spazio percepito attorno a sé; altri caratteristici sintomi dei pazienti con encefalopatia epatica sono le asterissi o flapping tremors, un tremore delle mani e delle braccia causato da una intermittente perdita del tono muscolare ed il tipico foetor hepaticus, causato dagli alti livelli di ammonio.
La gravità dell’encefalopatia epatica viene stabilita dai criteri di West Haven, che in base allo stato mentale, alla confusione, alla letergia, vengono divisi in quattro stadi (1-4), dal meno grave al più grave, come il coma epatico con assenza totale di risposta da parte del paziente. Il coma epatico è una condizione potenzialmente letale.
Nei pazienti affetti da cirrosi epatica, inoltre, è frequente anche lo sviluppo di una sindrome epato-renale, con una successiva probabilità di sviluppare insufficienza renale acuta ed alterazione elettrolitica, riferibile a iponatriemia ed ipokaliemia.
Il dramma della cirrosi epatica non riguarda solo la salute dei pazienti (salute sia fisica che psicologica) che ne viene inevitabilmente compromessa ma è anche un problema socio-economico-sanitario, riguardo le spese delle terapie medico-chirurgiche, delle ospedalizzazioni, delle giornate di lavoro perse, dell’inabilità che ne consegue.
Il carcinoma epatocellulare o epatocarcinoma (HCC) è uno dei tumori primitivi maligni del fegato che può essere un’altra conseguenza della cirrosi epatica; i noduli caratteristici della fibrosi vanno incontro ad un processo displastico con uno sviluppo anormale delle cellule epatiche fino a progredire ad uno stadio tumorale, che può essere ben differenziato fino ad arrivare ad un completo stato di indifferenziazione, generalmente più maligno ed aggressivo.

Trasmissione
La trasmissione del virus HCV e conseguentemente il silente instaurarsi dell’epatite C, avviene per via parenterale, attraverso il sangue e gli emoderivati. Il consumo di droghe per via endovenosa con l’utilizzo e lo scambio promiscuo di siringhe, le trasfusioni di sangue o i trapianti d’organo senza uno screening specifico per il virus, i tatuaggi con strumenti non monouso o precedentemente sterilizzati, sono tra le vie principali per la trasmissione e l’infezione del virus. In alcuni casi è stata dimostrata anche la trasmissione sessuale, anche se con una frequenza nettamente inferiore, per esempio, al virus HIV. La diffusione del virus HCV raggiunse il massimo picco intorno agli anni ’70 – metà anni ’80, periodo in cui le sacche di sangue che dovevano essere trasfuse non erano sottoposte a controlli infettivologici preventivi.
Epidemiologia
L’epatite C, prima della sua identificazione conosciuta come “epatite non A e non B“, è una patologia diffusa a livello mondiale, con alcuni paesi i cui dati sono particolarmente importanti (es. alcuni stati dell’Asia e dell’Africa). I dati aggiornati al 2020 riportati dall’Organizzazione Mondiale della Sanità riferiscono che nel mondo circa 70 milioni di persone sono affette da questa patologia e nel 2016 si stima che siano decedute circa 399 mila persone per le complicanze sia epatiche sia sistemiche indotte dal virus HCV. È bene ricordare però che i dati epidemiologici potrebbero non essere del tutto congruenti alla reale diffusione del virus, poiché la sua latenza non permette una diagnosi precoce ma solo quando sono presenti specifiche manifestazioni cliniche in uno stadio già avanzato.
Diagnosi
La diagnosi dell’epatite C viene eseguita con un semplice prelievo di sangue, a cui possono aggiungersi ulteriori analisi strumentali, solitamente per il monitoraggio e l’andamento dell’infezione precedentemente confermata.
Per la diagnosi vengono utilizzati saggi di laboratorio indiretti e diretti: i test indiretti, finalizzati alla ricerca degli anticorpi anti-HCV confermano un contatto col virus ma non indicano un eventuale fase attiva; il test diretto è senza dubbio più attendibile e specifico e riguarda invece la rilevazione del genoma virale, HCV-RNA quantitativo e qualitativo, in RT-Real Time PCR (RNA → cDNA). Successivamente alla rilevazione del genoma è di estrema importanza anche la genotipizzazione: il virus HCV è caratterizzato da una ampia ricombinazione genetica che gli conferisce la possibilità di avere diversi genotipi che in clinica vengono suddivisi in 1, 2, 3, 4, 5, 6: tali genotipi differenziano fra loro per distribuzione geografica ma soprattutto per sottoclasse e maggiore virulenza, infatti, tra questi sono conosciute le principali sottoclassi 1a, 1b, 2a, 2b, 3a, 4c e 4d. Il più diffuso, nonché il più virulento è l’1b. La genotipizzazione è svolta con una metodica di ibridazione inversa del DNA amplificato a sonde oligonucleotidiche specifiche adese su delle strisce di nitrocellulosa. La comparsa, dopo incubazione, di determinate colorazioni su tali strisce, permetterà la discriminazione di un certo genotipo rispetto ad un altro.
Test strumentali e di laboratorio
I test per la diagnosi ed il monitoraggio dell’epatite C possono essere sia strumentali sia di laboratorio e richiesti insieme, in determinate situazioni, possono essere di grande aiuto per avere il quadro clinico più completo.
- test di laboratorio: le analisi di laboratorio per valutare la presenza di epatite C e la funzionalità epatica vengono eseguite con tecniche di immunoenzimatica, tecniche di biologia molecolare e tecniche colorimetriche. In particolare, la ricerca del genoma virale viene eseguita in biologia molecolare con la RT-Real Time PCR che può dare un risultato quantitativo-qualitativo sulla presenza dell’HCV-RNA e la genotipizzazione per identificare il genotipo. In immunoenzimatica viene eseguita invece la ricerca degli anticorpi anti-HCV, mentre in chimica clinica vengono dosati altri parametri di funzionalità epatica come le proteine plasmatiche, in particolare l’albumina, la prealbumina e le proteine della coagulazione (indicatori di sintesi). Albumina e prealbumina sono ridotte, mentre il quadro elettroforetico si presenta con un caratteristico tracciato dove l’albumina è ridotta e le gamma globuline aumentate. Anche i fattori della coagulazione vanno incontro ad un deficit di sintesi, a causa dell’insufficiente assorbimento di vitamina K. Altri indicatori estremamente importanti nella valutazione della funzionalità epatica sono gli indicatori di coniugazione, come la bilirubina coniugata e non coniugata importante in presenza di ittero, gli indicatori di danno epatocellulare in cui rientrano le transaminasi, ALT ed AST; queste, sono specifiche di un danno ed una lesione epatocellulare: in particolare, l’incremento dell’enzima ALT è più marcato rispetto ad AST, poiché è espresso prevalentemente dal fegato. La concentrazione di ALT tende ad essere più alta nelle epatopatie acute, mentre elevati livelli di AST tendono ad essere riscontrati nelle epatiti croniche. Ulteriori indicatori richiesti ad analizzati anche in situazioni più avanzate, come la cirrosi epatica, sono la colinesterasi e l’ammoniemia nel sangue (iperammoniemia), il cui risultato è fondamentale per monitorare una situazione di encefalopatia epatica. Anche il dosaggio degli elettroliti, che spesso sono alterati, in particolare il sodio, può essere di aiuto per valutare in maniera più completa il quadro clinico di un paziente.
- test strumentali: i test strumentali vengono utilizzati per lo studio diretto del fegato, sia anatomico sia tessutale. In particolare, l’ecografia addominale è importante per studiare l’architettura dell’organo e rilevarne eventuali alterazioni, mentre negli stadi più avanzati tecniche come il fibroscan e la biopsia epatica sono significativi per valutare lo stadio di fibrosi. Inoltre nel caso di pazienti con cirrosi epatica e sospette varici esofagee la cui rottura può comportare un gravissimo sanguinamento digestivo, è opportuno eseguire anche una gastroscopia di controllo.
Terapia
Fino al 2013, lo schema terapeutico di elezione per il trattamento e l’eradicazione del virus HCV era l’utilizzo combinato dell’interferone e della ribavirina. Dal 2013, è iniziato l’utilizzo di nuovi farmaci ad attività antivirale diretta e specifica denominati Directly Acting Antivirals – DAA il cui meccanismo di azione è basato principalmente sull’inibizione dell’attività replicativa del virus, agendo direttamente sulle proteine che intervengono in quest’ultimo processo, come NS3, NS5A ed NS5B. Tali farmaci, quali ad esempio il Sofosbuvir, Simeprevir ed il Daclatasvir (utilizzati sempre in duplice terapia) sono risultati molto più efficaci e tollerati dai pazienti in cura, poiché andando ad agire in maniera diretta e specifica sui complessi di replicazione del virus, garantiscono una capacità di guarigione di oltre il 90 % anche nei pazienti affetti dal genotipo 1b, da sempre il più difficile da eradicare.
La sperimentazione di tali farmaci è ancora oggetto di studio, ma oltre alla terapia antivirale mirata – il cui dosaggio è fondamentale per disegnare un protocollo terapeutico il più possibile adeguato al paziente – è molto importante anche la terapia di supporto, soprattutto nei casi di epatite C in fase avanzata. Al fine di stabilire il corretto dosaggio del farmaco antivirale è necessario valutarne la concentrazione nel plasma, la cui misurazione viene eseguita con moderne tecniche di spettrometria di massa.
La terapia di supporto prevede la somministrazione di liquidi e di proteine plasmatiche, in particolare l’albumina che può essere somministrata singolarmente. In pazienti con encefalopatia epatica, che con opportuni presidi può essere opportunatamente trattata e resa reversibile, l’impiego di lassativo lattulosio per l’eliminazione delle sostanze tossiche presenti nell’intestino (ammonio) e la somministrazione di amminoacidi ramificati si è visto essere un valido aiuto per il miglioramento di tale condizione. Non sono attualmente presenti studi scientifici che accertino la reale validità di queste due terapie di supporto (lattulosio ed amminoacidi ramificati) ma sono le terapie ugualmente di scelta in situazioni di criticità ed emergenza. Il trapianto di fegato è generalmente l’ultima estrema scelta anche in caso di epatocarcinoma avanzato.
Conclusioni
L’epatite C è una patologia estremamente diffusa che interessa sia i pazienti colpiti sia i parenti dei pazienti stessi, che in situazioni avanzate si trovano completamente soli ed in uno stato di dolore ed afflizione. Questa patologia e tutte le complicanze sia fisiche sia psicologiche che ne derivano è una di quelle patologie che non dovrebbe mai essere dimenticata e messa da parte, poiché anche se è divenuta curabile con le nuove terapie, continua ad affliggere ancora molte persone e per questo non dovrebbe mai essere messa in secondo piano.
Per un futuro, senza epatite C.
Priscilla Caputi
Fonti
- Antonelli G., Clementi M. Principi di Virologia Medica. Casa Editrice Ambrosiana, 2018.
- Moroni M., Antinori S., Mastroianni C. Manuale di Malattie Infettive. Edra, 2020.
- Kenneth J. Ryan, C. George Ray. Sherris, Microbiologia Medica. The McGraw Hill Companies, 2017. Edizioni Mediche Scientifiche Internazionali.
- Cioffi M., Manuale di Diagnostica di Laboratorio. Edizioni Minerva Medica, 2010.
- Demarinis, S. (2020). Nobel Prize in Medicine Awarded for Discovery of Hepatitis C Virus. EXPLORE.
- Prasad, S., Dhiman, R. K., Duseja, A., Chawla, Y. K., Sharma, A., & Agarwal, R. (2007). Lactulose improves cognitive functions and health‐related quality of life in patients with cirrhosis who have minimal hepatic encephalopathy. Hepatology, 45(3), 549-559.
- https://www.thelancet.com/journals/lancet/article/PIIS0140-6736(20)32282-0/fulltext
- https://www.microbiologiaitalia.it/virologia/hepatitis-c-virus/
- https://www.epicentro.iss.it/epatite/aggiornamenti
- http://old.iss.it/pato/?lang=1&id=58&tipo=15
- https://www.epicentro.iss.it/epatite/epatite-c
- https://www.epicentro.iss.it/epatite/Epidemiologia-Mondo
- http://www.epac.it/
- http://www.epatitec.info/
- http://www.cirrosi.com/
- http://www.tumorefegato.it/patologia/tumori-maligni-primitivi/epatocarcinoma