Caratteristiche
Coccidioides immitis (Fig. 1) è un fungo che rientra nel phylum degli Ascomiceti, risiede primariamente nei terreni aridi e alcalini, dove si comporta come un saprofita, ed è un micete dimorfo, ossia è in grado di germinare assumendo due forme differenti a seconda del sito in cui si trova; nel suolo genera il micelio che rilascia le spore, mentre quando giunge ai polmoni forma delle strutture chiamate “sferule”. Inoltre, raffigura l’agente eziologico della malattia polmonare o sistemica chiamata coccidioidomicosi (detta anche Febbre di San Joaquin o Febbre della Valle).
C. immitis, come anche il parente C. posadasii, è diffuso prevalentemente nelle regioni desertiche degli Stadi Uniti d’America sudoccidentali come California, Arizona, New Mexico, Nevada, Texas e Utah (Fig. 2). Oltre a ciò, è endemico anche in alcuni stati dell’America meridionale come Brasile, Argentina, Colombia, Guatemala, Honduras, Messico, Nicaragua, Paraguay e Venezuela.


Dal punto di vista genetico, le due specie di Coccidioides possiedono genomi aploidi di 29 megabasi (Mb) contenenti pressappoco 10.000 quadri di lettura aperti (open reading frames, sequenze di DNA che vengono tradotte in proteine) su cinque cromosomi. Nonostante l’accoppiamento intraspecie e interspecie non sia mai stato osservato, il DNA di Coccidioides include i geni dell’accoppiamento, e in più subisce la ricombinazione genetica. C’è da dire che il 18% del genoma di Coccidioides è composto da DNA ripetuto, e in aggiunta a ciò sono presenti i trasposoni, che sono associati soprattutto con i geni codificanti per proteine che trasferiscono gruppi fosfato agli amminoacidi.
Nei miceti del genere Coccidioides le famiglie di geni codificanti per proteine chinasi e proteinasi, incluse subtilasi (famiglia di serina proteasi simili alla subtilisina) e cheratinasi (enzimi che decompongono la cheratina), sono ampliate rispetto alle specie strettamente correlate (Histoplasma capsulatum, Paracoccidioides spp. e Blastomyces dermatitidis), e ciò suggerisce che i funghi del genere Coccidioides possano essere specializzati nella crescita sulle proteine oltre che sui carboidrati.
Sfondo storico
La scoperta di questo micete risale al 1892 quando Alejandro Posadas, un medico specializzando dell’ospedale universitario di Buenos Aires, descrisse un soldato argentino di 36 anni che lamentava dei problemi dermatologici dal 1889, iniziati con una lesione alla guancia destra. Nel 1891, Posadas aveva visto per la prima volta il paziente, il quale presentava una massa grande, violacea e simil-fungina che gli copriva gran parte della guancia destra, diverse lesioni ulcerative sul naso, una sul braccio che ricordava un cavolfiore, e molte papule a livello del tronco e delle estremità. L’analisi di una biopsia cutanea rivelò la presenza di un organismo paragonabile ai protozoi Coccidi. Il paziente morì nel 1898 dopo sette anni di febbre ricorrente e lesioni cutanee progressive. Nel frattempo Posadas aveva inoculato il microorganismo in vari mammiferi, inclusi un cane, un gatto e una scimmia.
Un anno dopo il resoconto di Posadas, ci fu il caso di un operaio di 40 anni che si era trasferito dalle Azzorre alla Valle di San Joaquin in California; l’uomo si presentò all’ospedale di San Francisco con lesioni cutanee che progredirono fino a diventare orrendamente sfiguranti e distruttive, conducendo alla perdita degli occhi, del naso, del labbro superiore e di mezzo orecchio. Nessun trattamento riuscì a salvare il paziente, che morì nel 1895. L’autopsia permise di scovare numerosi noduli in svariati organi come polmoni, ghiandole surrenali, linfonodi, fegato, peritoneo, prostata, milza e testicoli. Dall’esame microscopico risultò che tali noduli erano granulomi, sovente con necrosi caseosa analoga a quella della tubercolosi, contenente organismi simili ai protozoi. Quando il paziente era ancora vivo, Emmet Rixford, un chirurgo del Cooper Medical College di San Francisco, effettuò un esperimento consistente nel suturare del tessuto infetto del paziente nel tessuto sottocutaneo di un coniglio. Ciò portò alla formazione di un’ulcera con rilascio di pus in cui era presente il microorganismo. In aggiunta a ciò, inoculò il tessuto infetto del paziente nella zampa di un cane, su cui comparve una lesione che si espanse, si ulcerò e liberò un essudato purulento ricco di microorganismi.
Nel 1896, Thomas Caspar Gilchrist, coautore del rapporto di Rixford, esaminò il materiale e concluse che il microorganismo era un protozoo affine ai Coccidi. Gilchrist e Rixford, insieme al parassitologo C. W. Stiles, nominarono tale microorganismo Coccidioides (somigliante ai Coccidi) immitis (“not mild”, che significa non leggero).
La teoria di Gilchrist venne confutata quattro anni dopo grazie a William Ophüls e Herbert Charles Moffitt, i quali coltivarono un campione prelevato da un altro paziente in California. Dalla coltura crebbe una muffa che all’inizio Ophüls considerò un contaminante. Tuttavia, i due scienziati introdussero il tessuto e il pus del paziente nel peritoneo di porcellini d’India, e isolarono il microorganismo dagli organi infetti. Dopodiché iniettarono il micete derivato dalla coltura in un coniglio, nel quale si svilupparono i noduli contenenti i microorganismi visibili in diversi tessuti. Tali esperimenti dimostrarono che C. immitis non era un protozoo, bensì un fungo che esisteva in due forme: colonie miceliali in coltura e corpi sferici simili a protozoi (le sferule) nei tessuti in cui si riproducono.
Filogenesi
Dominio Eukaryota
Regno Fungi
Phylum Ascomycota
Classe Eurotiomycetes
Ordine Onygenales
Famiglia Onygenaceae
Genere Coccidioides
Specie C. immitis
Morfologia e ciclo vitale
Come abbiamo descritto in precedenza, C. immitis può assumere due conformazioni. Partendo da quella che si sviluppa nei terreni di coltura, ovvero la muffa, a livello macroscopico le colonie si presentano ampie, bianco-grigiastre e dall’aspetto soffice (Fig. 3). Al livello microscopico, invece, è caratterizzato da spore di forma quadrata-rettangolare di 2-4 μm di diametro, chiamate artroconidi, che appaiono separate da uno spazio vuoto che rimane incolore dopo l’applicazione della colorazione (Fig. 1 e 4).


Per quanto concerne la configurazione che viene acquisita all’interno degli organismi ospiti, microscopicamente il fungo è contraddistinto da strutture rotondeggianti, conosciute come sferule, all’interno delle quali maturano delle cellule asessuali, resistenti all’ambiente esterno, dette endospore (Fig. 5).

I funghi del genere Coccidioides compiono un ciclo asessuato che comprende due stadi, ovvero saprofita e parassita (Fig. 6). Nella prima fase, il micete, presente nel suolo, genera il micelio che libera gli artroconidi, i quali si disperdono nell’aria e possono essere inalati da un potenziale ospite suscettibile; in caso contrario rimangono nell’ambiente esterno e continuano il ciclo saprofitico. Se le spore penetrano in un organismo, si ingrandiscono e si differenziano in sferule che, nel giro di 24-72 ore, vanno incontro a divisione nucleare e iniziano lo sviluppo delle endospore (stadio parassitario). In un lasso di tempo di 72-120 ore le sferule mature si rompono e sprigionano le endospore, ognuna delle quali può creare una nuova sferula, oppure, in caso di bassa temperatura, particolari condizioni atmosferiche o cambiamenti dei nutrienti, può convertirsi in micelio e ricominciare lo stadio saprofitico.

Patogenesi
Abbiamo già detto che la patologia causata da C. immitis (e anche dal C. posadasii) è la coccidioidomicosi, che può coinvolgere solo i polmoni oppure svilupparsi come una malattia disseminata a causa della possibile diffusione del microorganismo per via ematica. L’infezione avviene successivamente all’inalazione degli artroconidi liberati nell’aria dal micelio; questi raggiungono gli alveoli polmonari, dove le cellule immunitarie riconoscono i componenti fungini mediante diversi recettori, dopodiché le spore vengono fagocitate da macrofagi non fungicidi. Nel giro di alcune ore gli antigeni del micete stimolano un afflusso di granulociti neutrofili, i quali possono incrementare la formazione delle sferule. I granulociti neutrofili rispondono all’incontro con gli artroconidi in maniera similare ai macrofagi, ossia li inglobano senza ucciderli. Ciò è associato al fallimento della fusione del fagosoma con il lisosoma, garantendo quindi la protezione delle spore dal contatto con gli enzimi lisosomiali.
Quando le spore si convertono in sferule, invadono i tessuti, si ingrandiscono e vanno incontro a rottura con conseguente rilascio di endospore, che possono dare origine a ulteriori sferule. La figura 7 riassume sommariamente il ciclo dell’infezione.
La diffusione di C. immitis, e le conseguenti epidemie, si realizza più facilmente quando giornate aride e ventose accompagnano forti piogge, che favoriscono la proliferazione del micelio. I fattori che accentuano il rischio di coccidioidomicosi sono l’indebolimento del sistema immunitario (legato all’AIDS, a malattie ematologiche o all’impiego di farmaci immunosoppressori), l’emodialisi, l’età avanzata, il secondo semestre di gravidanza, alcune professioni come l’agricoltura e l’edilizia, e l’appartenenza a determinate etnie come filippini, afroamericani, nativi americani, ispanici e asiatici.

Dal punto di vista della sintomatologia, la Febbre della Valle ha un’incubazione da sette a ventuno giorni e si distingue in polmonare, cutanea e disseminata. Il 60% degli individui affetti da coccidioidomicosi polmonare è asintomatico, mentre il restante 40% può manifestare una malattia respiratoria simil-influenzale, bronchite acuta o, meno frequentemente, polmonite acuta o versamento pleurico. I sintomi includono febbre, emicrania, tosse, dolore toracico, brividi, dolore faringeo ed emottisi (tosse con emissione di sangue).
La malattia polmonare è distinta da una reazione infiammatoria mediata dai granulociti neutrofili, produzione di pus e formazione di granulomi (coccidioidomi) in cui il micete appare sotto forma di grosse sferule contenenti endospore (Fig. 8), facilmente visibili mediante colorazioni a impregnazione argentica (Fig. 8B). Si ha la formazione di lesioni polmonari primarie, che lasciano, a volte, delle lesioni nodulari a moneta. Queste potrebbero essere confuse con tumori, tubercolosi o altre infezioni granulomatose (è fondamentale quindi effettuare una corretta diagnosi differenziale). In aggiunta a ciò, possono comparire delle lesioni cavitarie, connesse all’infiltrazione neutrofila secondaria, che col tempo variano di dimensioni e in genere sono racchiuse da una parete fibrotica sottile. Queste lesioni possono rimarginarsi per fibrocalcificazione o in alternativa evolvere verso la creazione di cavità parenchimali di maggiori dimensioni, chiamate “grandi cavità residue”, che spesso contengono liquido. Esse raffigurano l’inizio di pneumopatie evolutive di vario tipo e in una ristretta percentuale di casi non guariscono in maniera spontanea.

La coccidioidomicosi cutanea può essere parte dell’infezione polmonare acuta e scatenarsi come un esantema polmonare acuto, riflettere la presenza di un’infezione disseminata (in questo caso si parla di infezione cutanea secondaria), oppure presentarsi come un’infezione primaria dovuta a inoculazione diretta, ma tale evento è alquanto raro. I sintomi a livello della pelle sono classificati come reattivi, si verificano durante la malattia polmonare primaria in più del 50% dei pazienti, e comprendono l’eritema nodoso, l’eritema multiforme, l’esantema acuto generalizzato, la dermatite granulomatosa interstiziale e la sindrome di Sweet.
L’eritema nodoso rappresenta la manifestazione cutanea reattiva più comune, compare dopo un periodo che va da una a tre settimane dall’inizio dei sintomi respiratori. Si tratta di un disordine della cute e dei tessuti sottocutanei con noduli eritematosi e dolorosi localizzati normalmente alle estremità (Fig. 9).
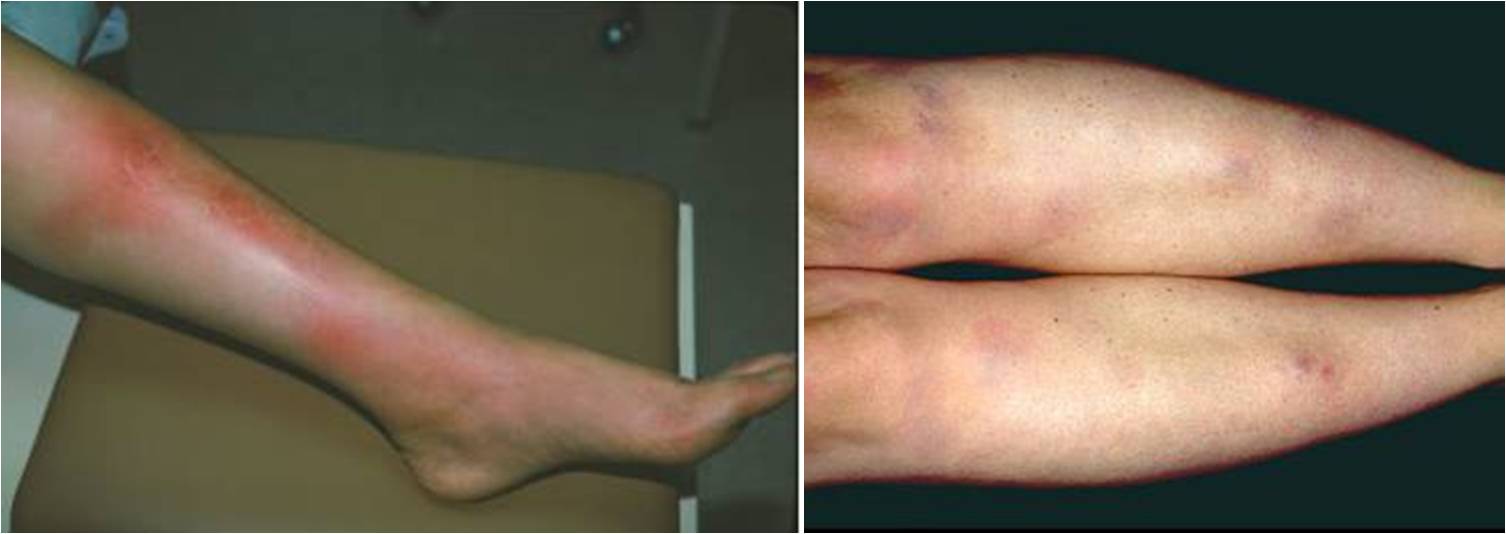
L’eritema multiforme è caratterizzato da varie tipologie di lesioni come ponfi, macule eritematose, papule o vescicole. Le lesioni classiche esibiscono un centro violaceo circondato da un alone separato da un anello pallido (lesioni a bersaglio), e si formano nel giro di 48 ore dai primi sintomi (Fig. 10).
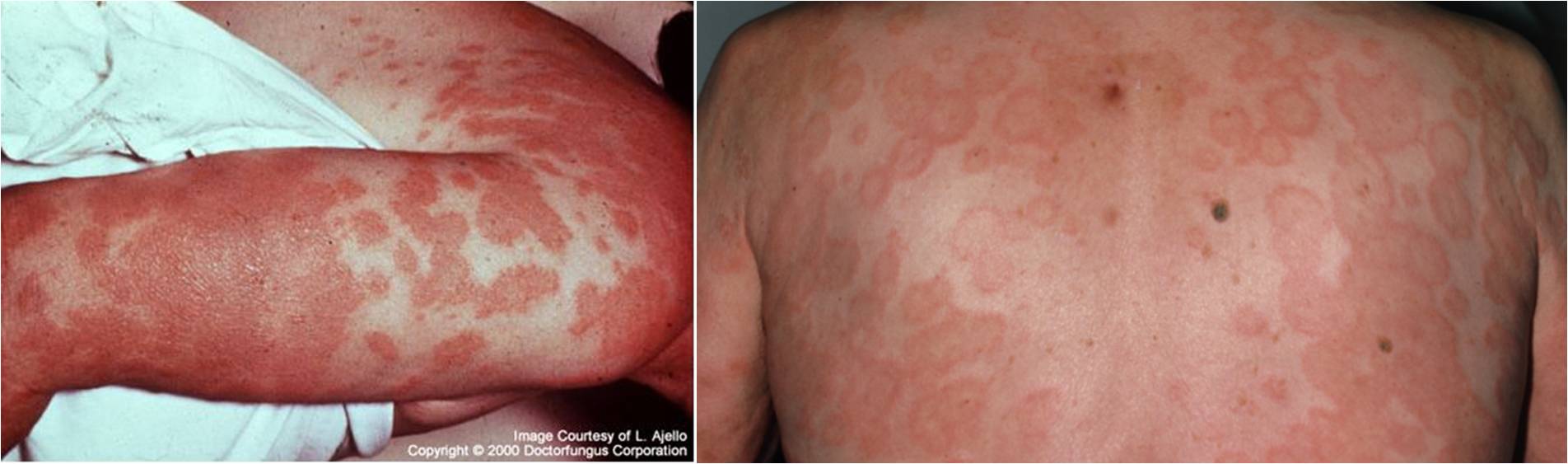
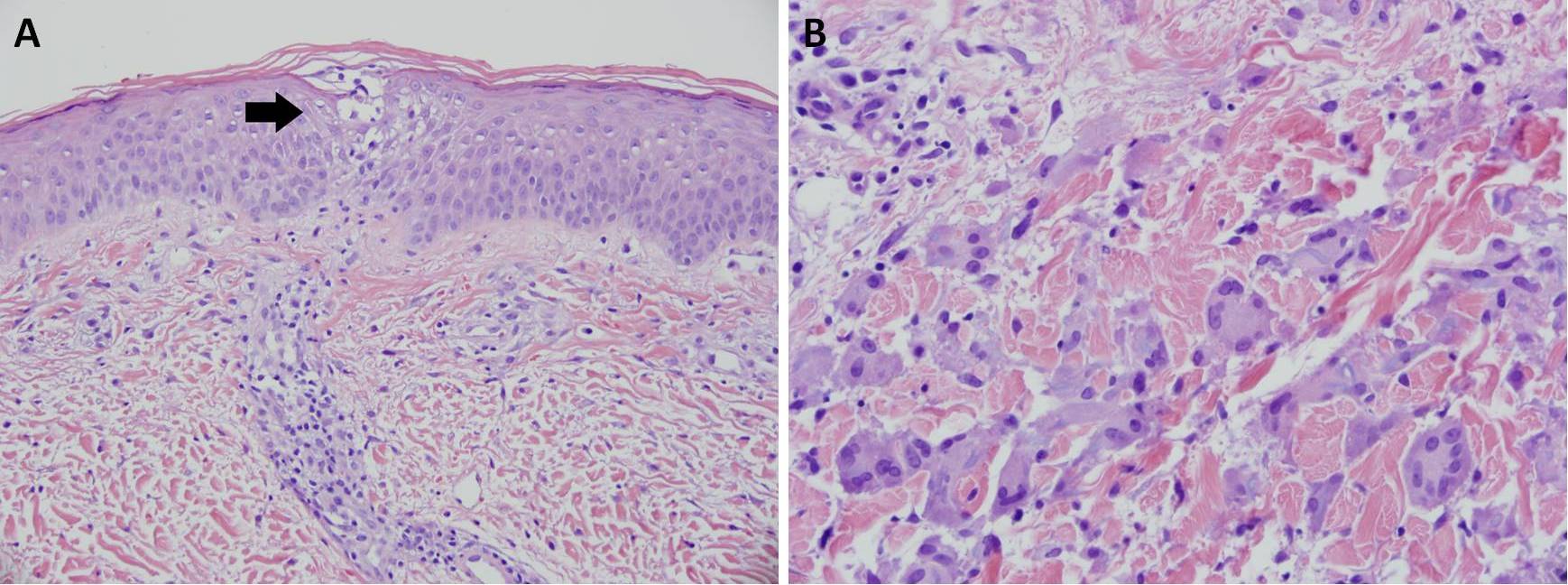
L’esantema acuto insorge con eruzioni cutanee come macule, papule o lesioni morbilliformi che possono essere pruriginose e permanere per diverse settimane. Questo tipo di patologia può essere confusa con la dermatite da contatto o l’eritema multiforme. A livello istologico si nota una spongiosi media dell’epidermide (siero nello strato spinoso che comporta il distacco delle cellule e la creazione di cavità nello spessore dell’epidermide) e un infiltrato infiammatorio perivascolare con linfociti, neutrofili ed eosinofili (Fig. 11 A). In alcune circostanze l’esantema può essere seguito da desquamazione dei palmi delle mani.
Per quanto concerne la dermatite granulomatosa interstiziale, è stata documentata in cinque pazienti con coccidioidomicosi polmonare, e le lesioni tipiche sono papule, noduli e placche, che si risolvono in un periodo di tempo variabile, da qualche giorno a due mesi. L’esame istologico mostra un infiltrato interstiziale del derma con istiociti mescolati con neutrofili, eosinofili e cellule giganti multinucleate (Fig. 11 B).
Parliamo infine della sindrome di Sweet (o dermatosi neutrofila acuta febbrile), che è una forma di coccidioidomicosi alquanto inconsueta contraddistinta da febbre, leucocitosi neutrofila, papule eritematose doloranti e placche, che compaiono sulle braccia, sul viso e sul collo (Fig. 12).

Per concludere questa parte, descriviamo la coccidioidomicosi disseminata, che si verifica in una percentuale di individui tra l’1% e il 5%, insorge normalmente entro due anni dall’esposizione, e le persone affette lamentano febbre, tosse, dispnea ed escreato muco-purulento o ematico. Il microorganismo può diffondersi mediante il circolo ematico e arrivare in qualsiasi organo, anche se quelli più abitualmente colpiti sono la cute, il sistema nervoso centrale, le ossa e le articolazioni. Partendo dal coinvolgimento della pelle, i pazienti possono presentare una lesione singola oppure lesioni cutanee multiple (tra cui pustole, papule, vescicole, noduli, placche, ascessi sottocutanei), con o senza ulcerazione (Fig. 13). Le zone interessate in maggior misura sono la testa, il tronco e le estremità.
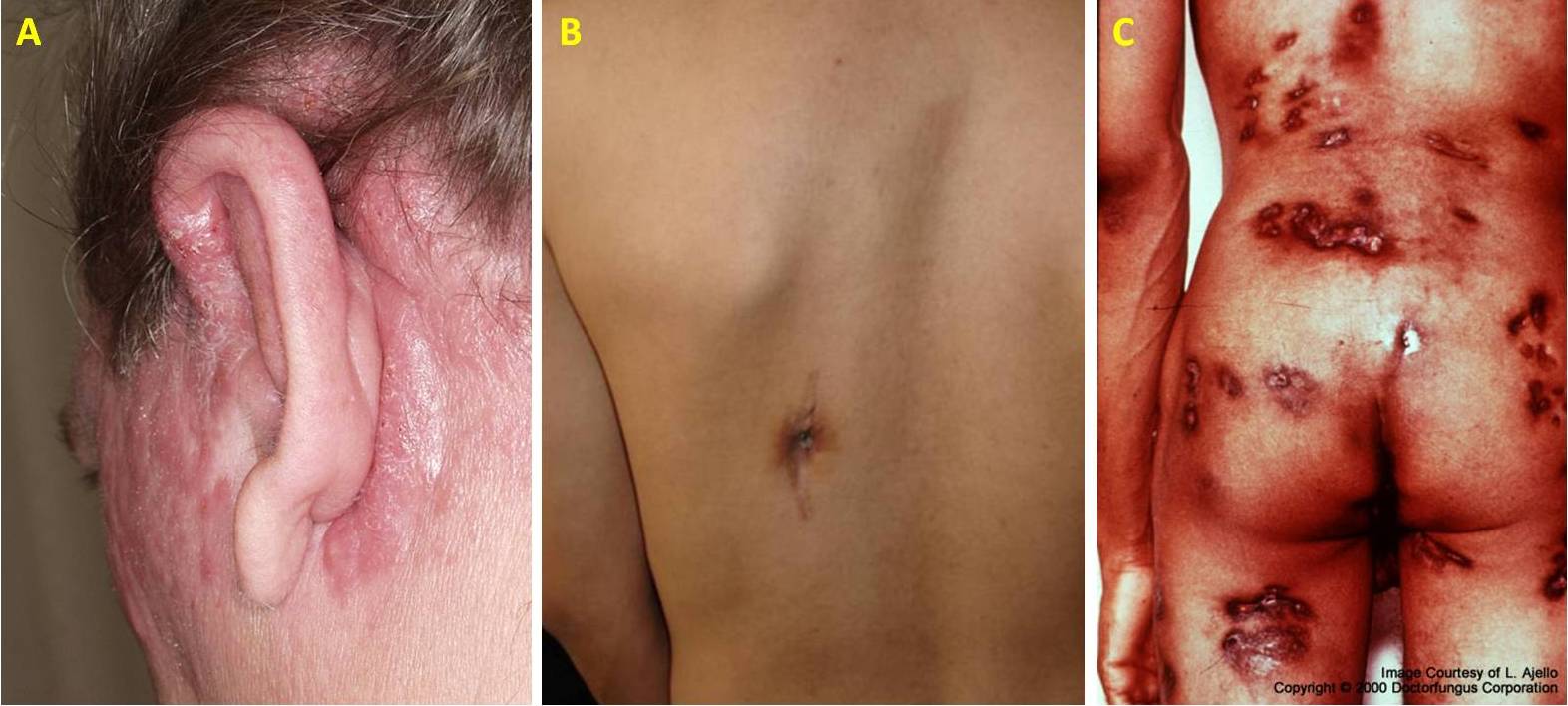
Per quanto concerne l’implicazione dell’apparato scheletrico e del sistema nervoso centrale, la prima condizione riguarda il ginocchio o le vertebre, si manifesta con tumefazione graduale, calore, arrossamento e dolore sordo, e può essere difficile da curare. La seconda provoca la meningite, che è fatale se non viene trattata con una terapia prolungata (il 95% dei pazienti muore nel giro di due anni dalla diagnosi).
Uno sguardo all’immunologia
Nell’infezione da Coccidioides la risposta immunitaria vede come maggiori protagonisti le cellule fagocitiche, ovvero macrofagi e neutrofili, che sono in grado di inglobare gli artroconidi, le sferule iniziali e le endospore, ma non riescono a fagocitare le sferule mature a causa delle grosse dimensioni (20-100 µm). Il micete stabilisce una relazione sia extracellulare che intracellulare con le cellule dell’organismo ospite; c’è da sottolineare che le cellule fagocitiche sono sottoposte a uno stress elevato, poiché devono ampliare la loro superficie allo scopo di contenere le grandi sferule durante la fagocitosi.
Come avevamo già accennato, le endospore liberate dalle sferule stimolano un’affluenza di neutrofili, che rappresentano la componente più abbondante del sistema immunitario innato e che risponde più rapidamente.
Il microorganismo ha la capacità di sopravvivere all’attacco da parte delle cellule fagocitiche attraverso multiple strategie. Una di queste è l’espressione di una metalloproteasi (Mep1) che degrada una glicoproteina presente sulla parete esterna delle sferule (SOWgp). Questa molecola raffigura il principale antigene di superficie, quindi un bersaglio rilevante dell’immunità; si è visto che, in vitro, l’opsonizzazione delle cellule fungine con anticorpi policlonali anti-SOWgp aumenta la fagocitosi e l’eliminazione da parte dei macrofagi. Un’altra strategia messa in atto da Coccidioides è la soppressione della sintesi di ossidanti antimicrobici come il perossido d’idrogeno, l’acido ipocloroso e l’ossido nitrico.
Oltre ai macrofagi e ai neutrofili, alla reazione immunitaria verso Coccidioides partecipano anche le cellule dendritiche, che sono un ponte tra la risposta immunitaria innata e quella adattativa; esse catturano, processano gli antigeni provenienti dal fungo e promuovono lo sviluppo e il differenziamento dei linfociti per dare inizio alla risposta immunitaria acquisita. Giocano un ruolo cruciale nella presentazione degli antigeni e nell’attivazione dei linfociti durante la coccidioidomicosi. Andando più in dettaglio sull’instaurazione dell’immunità acquisita, le cellule dendritiche e i macrofagi riconoscono i componenti espressi sulla superficie delle endospore (carboidrati, lipidi e proteine) mediante tre tipi di recettori, ovvero i recettori di tipo Toll (TLRs), i recettori della lectina di tipo C (CLRs) e i recettori di tipo NOD (NODs). L’interazione antigeni-recettori attiva delle specifiche vie di segnalazione (Card9 e Myd88) che innescano la trascrizione di geni codificanti per citochine pro-infiammatorie come interferone gamma (INF-γ), interleuchina 1β (IL-1β) e interleuchina 23 (IL-23). Queste inducono il differenziamento dei linfociti T CD4 in linfociti Th1 e Th17, che lavorano in maniera sinergica per eliminare l’agente patogeno incrementando il reclutamento dei fagociti negli alveoli e promuovendo la riduzione della quantità di Coccidioides mentre smorzano l’infiammazione nei siti di infezione. Il processo è riassunto in Figura 14.

Metodi di identificazione
L’approccio diagnostico della Febbre della Valle consta soprattutto di tre metodiche, ossia l’analisi microscopica, l’esame colturale e i saggi sierologici.
L’osservazione al microscopio ottico consente di avvistare le sferule del fungo in vari tipi di campioni come espettorato, liquido pleurico, liquido cerebrospinale, biopsie polmonari o cutanee; tali campioni possono essere colorati con Ematossilina-Eosina, oppure con colorazioni che aiutano a far risaltare meglio il microorganismo, e tra queste abbiamo la reazione PAS (acido periodico di Schiff) e il metodo di Grocott-Gomori. Le sferule hanno una dimensione che va da 10 a 80 μm e, nel caso di coccidioidomicosi cutanea, si trovano nella parte superiore del derma. In quelle più mature talvolta si distinguono numerose endospore, e tale caratteristica permette di differenziare la coccidioidomicosi dalla blastomicosi.
L’esame colturale si effettua seminando il campione su svariati terreni come agar sangue, agar cioccolato, Sabouraud Dextrose agar (SDA) e Brain Heart Infusion agar (BHI) . La crescita del fungo avviene a temperatura ambiente e può impiegare da 2 a 7 giorni o da 2 a 3 settimane.
I test sierologici permettono di dosare gli anticorpi IgM e IgG contro gli antigeni fungini; sono metodiche altamente sensibili e specifiche, e includono i saggi immunoenzimatici, il test di fissazione del complemento (usato per rilevare le IgG), il test di precipitazione e il test di immunodiffusione (utilizzati per individuare le IgM). Il test di fissazione del complemento effettuato sul liquido cefalorachidiano è utile e fondamentale al fine di diagnosticare la meningite da Coccidioides, in quanto la coltura di tale campione è raramente positiva.
Ulteriori tecniche diagnostiche sono la ricerca dell’antigene urinario, che si adopera nei pazienti immunodepressi colpiti da polmonite e infezione disseminata.
Infine, ci sono i test molecolari come l’ibridazione in situ (ISH) e la reazione a catena della DNA polimerasi (PCR), che consentono di riscontrare il DNA del microorganismo. Tuttavia, non sono ampiamente disponibili e la loro sensibilità non è stata determinata.
Terapia
Il trattamento della coccidioidomicosi si basa sull’impiego di farmaci differenti a seconda della gravità e del tipo di patologia:
- Se abbiamo di fronte una malattia polmonare primaria o una malattia extrapolmonare lieve-moderata, senza coinvolgimento delle meningi, il trattamento consiste in fluconazolo orale 400 mg una volta al giorno, o itraconazolo orale 200 mg due volte al giorno, per un periodo di 3 o 6 mesi;
- In caso di malattia severa, si somministra amfotericina B 0,5-1 mg/kg una volta al giorno per 4-12 settimane;
- Per i pazienti con coccidioidomicosi associata all’AIDS, la terapia costa di fluconazolo orale 200 mg una volta al giorno o itraconazolo 200 mg due volte al giorno, e continua fino a quando la conta dei linfociti CD4 arriva a >250 cellule/μl;
- Se la coccidioidomicosi colpisce le meningi, il farmaco da utilizzare è il fluconazolo orale, con dosi di 800-1200 mg una volta al giorno, e questa terapia deve proseguire per tutta la vita.
L’itraconazolo e il fluconazolo bloccano la 14-alfa-demetilasi, un enzima che catalizza la sintesi dello steroide ergosterolo, un componente primario della membrana cellulare fungina. L’amfotericina B, invece, agisce penetrando nella membrana dei miceti, e ciò ne compromette la permeabilità.
Nel caso in cui le lesioni cavitarie residue provocano emottisi o rischiano di rompersi nello spazio pleurico, la soluzione migliore è l’intervento chirurgico.
Fonti
- Theo N. Kirkland and Joshua Fierer. 2018. “Coccidioides immitis and posadasii; A review of their biology, genomics, pathogenesis, and host immunity”, Virulence
- Jan V. Hirschmann. 2007. “The Early History of Coccidioidomycosis: 1892–1945”, Clinical Infectious Diseases
- Frederick S. Fisher, Mark W. Bultman and Demosthenes Pappagianis. 2000. “Operational Guidelines (version 1.0) for Geological Fieldwork in Areas Endemic for Coccidioidomycosis (Valley Fever)”, USGS
- Eric R. G. Lewis, Jolene R. Bower and Bridget M. Barker. 2015. “Dust Devil: The Life and Times of the Fungus That Causes Valley Fever”, PLOS Pathogens
- J.E. Carrasco-Zuber, C. Navarrete-Dechent, A. Bonifaz, F. Fich, V. Vial-Letelier, D. Berroeta-Mauriziano. 2016. “Cutaneous involvement in the Deep Mycoses: A Review. Part II—-Systemic Mycoses”, Actas Dermosifiliogràficas
- Libero Ajello, Claudio Farina, Aldo Mazzoni e Giuseppe Picerno. 1993. “Fondamenti di micologia clinica”, AMCLI
- Natalia Castro-Lopez and Chiung-Yu Hung. 2017. “Immune Response to Coccidioidomycosis and the Development of a Vaccine”, Microorganisms