I folati sono conosciuti anche come vitamina B9 e negli esseri viventi sono necessari per la sintesi dei nucleotidi del DNA e dell’RNA (Figura 1), e quindi anche per la conservazione e la trasmissione dell’informazione genetica. Per questa ragione sono particolarmente abbondanti nei tessuti “giovani” dove è attiva la divisione cellulare o per cui è necessario il ricambio delle cellule morte, e anche negli organismi unicellulari. Pertanto sono fonti di folati, vitamine già in forma attiva, le foglie verdi, i semi, le uova, il latte, la pelle, le mucose, il lievito e la flora intestinale. Tuttavia per motivi igienici, molti di questi alimenti non possono essere consumati crudi e comunque i folati si degradano alle alte temperature e si perdono con l’acqua di cottura, poiché sono idrosolubili.

Folati e acido folico
Per poter fornire una quantità sufficiente di folati attraverso l’alimentazione, molti cibi sono fortificati con una forma artificiale di vitamina B9, prodotta chimicamente, chiamata acido folico. L’acido folico, a differenza dei folati naturali, è più stabile al calore, ma deve subire alcune reazioni biochimiche per acquisire la forma attiva. Questo articolo percorre idealmente le principali reazioni che coinvolgono i folati: partendo dalla loro sintesi nei vegetali, passando per l’assorbimento intestinale, la loro assimilazione e attivazione, la loro funzione nel metabolismo dei nucleotidi e degli aminoacidi, per finire con la loro eliminazione ed escrezione.
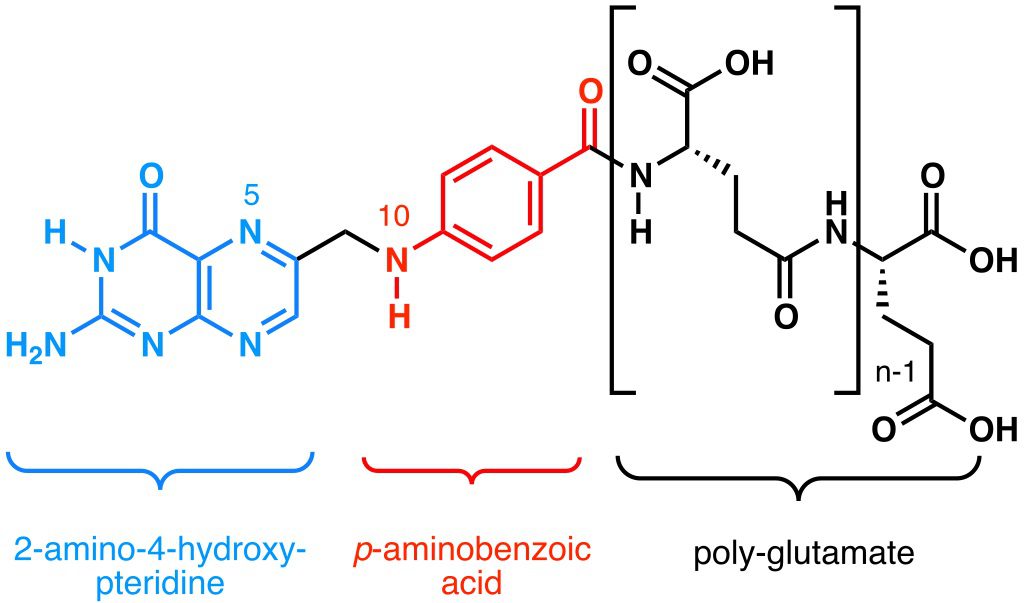
I folati hanno una formula chimica complessa, che si compone di tre parti (Figura 2):
- una pterina, formata da un doppio anello di atomi di carbonio e azoto;
- un’unità di acido p-amminobenzoico (pABA);
- una coda formata da unità di acido glutammico.
Biosintesi dei folati
Il metabolismo degli animali non riesce a produrre i folati, e per questo motivo essi devono assumerli attraverso l’alimentazione. Invece piante, funghi e batteri riescono a sintetizzarne, legando tra loro le tre parti. Nelle piante la sintesi dei folati vede la partecipazione di tre distinti compartimenti della cellula.
- la produzione della pterina avviene nel citosol, a partire dal nucleotide GTP;
- la sintesi del pABA si svolge nei plastidi
- l’assemblaggio dei folati si conclude nei mitocondri con l’unione tra pterina e pABA, e l’aggiunta della coda di poli-glutammato.
- La quantità di folato disponibile per le reazioni della cellula vegetale è regolata immagazzinando nel vacuolo le riserve di folato al momento inattive.
La sintesi dei folati da parte dei batteri merita una menzione, perché questa via metabolica rappresenta il bersaglio di una rilevante categoria di antibiotici: i sulfamidici.
Digestione, assorbimento intestinale e circolazione
Quando un animale assume un alimento contenente folati, gli enzimi del suo intestino accorciano la coda di poli-glutammato fino a lasciare una o due unità di questo aminoacido. Così facendo nel duodeno e nel digiuno può avvenire l’assorbimento dei folati privati della coda. In seguito i folati entrano nella circolazione sanguigna e qui vengono trasportati dai globuli rossi o da apposite proteine oppure disciolti nel plasma.
Attivazione
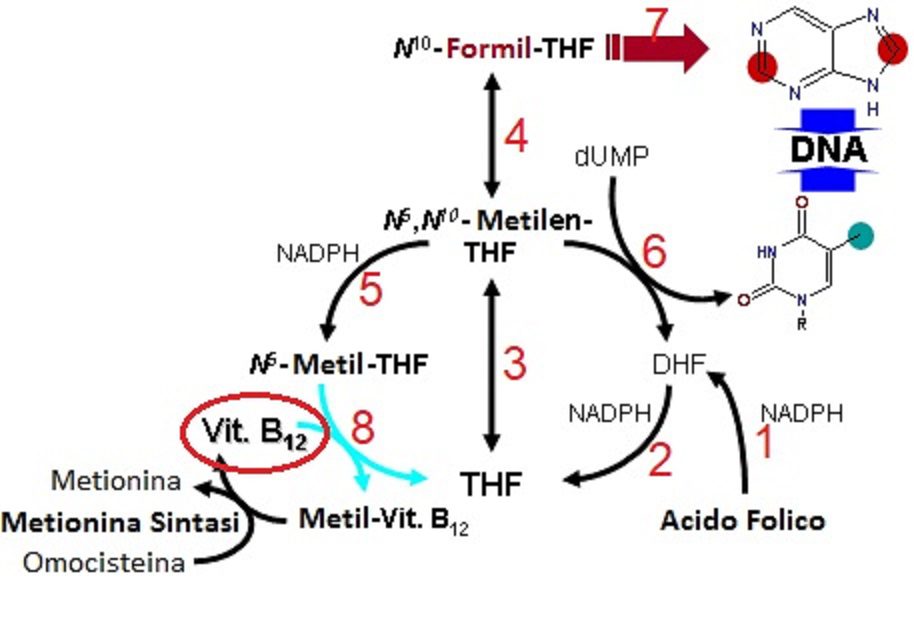
Quando i folati raggiungono l’interno delle cellule, soprattutto quelle del fegato, queste li immagazzinano sotto forma di poli-glutammati. Tuttavia in caso di necessità, si rimuove (o si accorcia) la coda e l’acido folico subisce due successive riduzioni con l’aggiunta di quattro atomi di idrogeno (Figura 3, passaggi 1 e 2). Da questa via metabolica si ottiene, il tetraidrofolato (THF), che è la forma attiva del metabolismo dei folati, indispensabile per il funzionamento di alcuni enzimi. Grazie al THF è possibile aggiungere o rimuovere da opportune molecole dei gruppi di atomi con un solo atomo di carbonio. Queste reazioni coinvolgono due atomi di azoto (N5 e N10) del THF, i quali possono accettare e donare questi gruppi.
Il THF come accettore
Dopo la sua attivazione il THF accetta un gruppo metilene (-CH2-) proveniente dalla catena laterale dell’aminoacido serina, attraverso una reazione che converte la serina in glicina (Figura 3, passaggio 3). Questa reazione richiede l’intervento di un’altra vitamina del gruppo B, cioè il piridossalfosfato (PLP). Nei successivi passaggi, questo metilene può:
- essere donato tal quale ad altre molecole,
- subire ossidazione a gruppo formile (-CHO) (Figura 3, passaggio 4),
- subire riduzione a gruppo metile (-CH3) (Figura 3, passaggio 5).
Ognuna di queste forme di folato è quindi responsabile di importanti vie metaboliche.
Il THF come donatore
- La forma di THF, che lega il gruppo metilene, trasferisce questo gruppo al dUMP che diventa dTMP, sintetizzando così la Timina, una base azotata presente solamente nel DNA (Figura 3, passaggio 6). Questa reazione è particolarmente importante, poiché una carenza di folati nell’alimentazione provoca l’anomala incorporazione di dUMP nel DNA, con conseguenti mutazioni geniche, responsabili dell’insorgenza di disfunzioni e tumori. Nei tumori la velocità di replicazione cellulare è aumentata e perciò vi è un’intensa attività degli enzimi che rigenerano ciclicamente il THF. Questi enzimi sono quindi il bersaglio dell’azione di molti farmaci chemioterapici.
- Il gruppo formile contribuisce alla sintesi dei nucleotidi AMP e GMP, inserendo così in due distinti passaggi il proprio atomo di carbonio nella costruzione del doppio anello delle basi puriniche Adenina e Guanina (Figura 3, passaggio 7).
- Il gruppo metile, invece serve a “tamponare” l’eccesso di omocisteina, un aminoacido potenzialmente dannoso per la circolazione sanguigna. Il trasferimento del metile, grazie all’intervento della vitamina B12, trasforma l’omocisteina in metionina (Figura 3, passaggio 8). La metionina in seguito cede il gruppo metile per modificare chimicamente acidi nucleici, proteine, lipidi e neurotrasmettitori, ritrasformandosi in omocisteina. Una carenza di vitamina B12 determina il blocco di questa via metabolica, poiché il THF rimane nella forma metilata senza poter ritornare alla forma attiva THF. Questa situazione di stallo induce quindi una carenza secondaria di THF nota come “trappola dei folati”.
Eliminazione dei folati
La quantità di folati in eccesso, rispetto alle esigenze dell’organismo, viene eliminata in due modi.
- Una parte dei folati viene escreta dal fegato con la bile e può tornare al fegato attraverso il circolo enteroepatico o essere quindi espulsa dall’organismo con le feci assieme ai folati che non sono stati assorbiti e a quelli prodotti dalla flora intestinale.
- La maggior parte dei folati, invece, è rimossa dalla circolazione sanguigna attraverso l’ultrafiltrazione renale ed è eliminata con le urine.
Fonti:
- Halsted CH. The intestinal absorption of folates. Am. J. Clin. Nutr. 1979;32(4):846–55.
- Scott JM, Weir DG. The methyl folate trap. A physiological response in man to prevent methyl group deficiency in kwashiorkor (methionine deficiency) and an explanation for folic-acid induced exacerbation of subacute combined degeneration in pernicious anaemia. Lancet. 1981;2(8242):337-40.
- Scott JM. Folate and vitamin B12. Proc Nutr Soc. 1999;58(2):441-8.
- Fenech M. The role of folic acid and Vitamin B12 in genomic stability of human cells. Mutat Res. 2001;475(1-2):57-67.
- Patrizia Cappelli, Vanna Vannucchi; Chimica degli alimenti – Terza edizione 2005; Zanichelli; ISBN 978-88-08-07589-5.
- Herrmann W. Significance of hyperhomocysteinemia. Clin Lab. 2006;52(7-8):367-74.
- David L. Nelson, Michael M. Cox; Lehninger: Principles of Biochemistry – 6th Edition 2013, 2008, 2005, 2000; W.H. Freeman and Company, New York; ISBN 978-88-08-62118-4.
- Gorelova V, Bastien O, De Clerck O, Respinats S, Rébeillé F, Van Der Straeten B. Evolution of folate biosynthesis and metabolism across algae and land plant lineages. Sci Rep. 2019;9:5731.
Crediti immagini
- Immagine in evidenza: https://cdn.gvmnet.it/admingvm/media/immagininews/ghiandoleeapparatoendocrino/vitamina_b9_benefici_gravidanza.jpeg
- Figura 1: https://www.chimica-online.it/biologia/immagini/differenze-tra-dna-e-rna.jpg
- Figura 2: https://upload.wikimedia.org/wikipedia/commons/e/e9/Folate_family.svg
- Figura 3: https://www.freelandtime.com/images/B9B12.png