Le CAR-T (Chimeric Antigen Receptor T cell therapies, ovvero Terapie a base di cellule T esprimenti un Recettore Chimerico per antigene) sono innovative terapie geniche per la cura contro il cancro. Agiscono direttamente sul sistema immunitario del paziente, rendendolo in grado di riconoscere e distruggere le cellule tumorali. Le CAR-T rientrano tra le più innovative terapie avanzate, frutto dei progressi scientifici nel campo della biotecnologia molecolare.
Terapia genica
La terapia genica CAR-T si basa sulla modifica e sul potenziamento dei linfociti T, i quali riconoscono e aggrediscono le cellule tumorali (Fig.1). La terapia agisce attraverso l’inserzione di materiale genetico all’interno delle cellule dell’organismo umano.
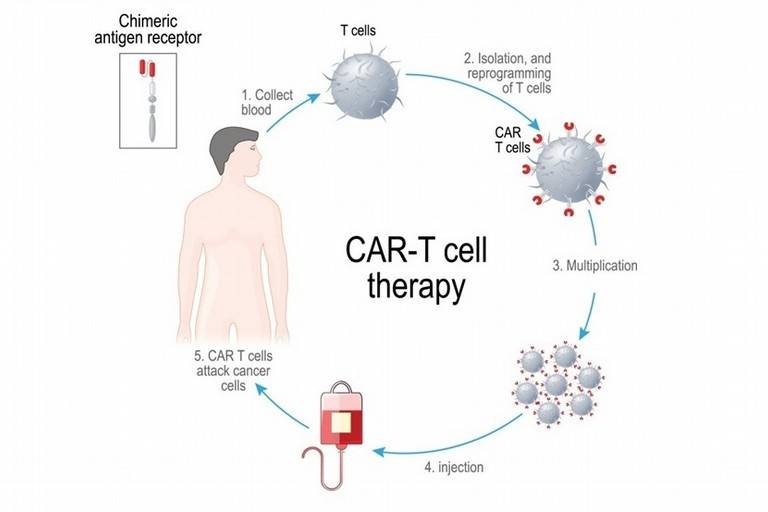
Tramite un semplice campione ematico si estraggono i linfociti T del paziente che sono modificati geneticamente e coltivati in laboratorio. Attraverso complessi processi di ingegnerizzazione si introduce un recettore CAR (Chimeric Antigen Receptor) capace di riconoscere le cellule tumorali (Fig.2). I linfociti così modificati vengono poi re-infusi nel paziente da cui sono estratti precedentemente. Grazie alla proteina di superficie, i linfociti T riconoscono uno specifico bersaglio, come l’antigene CD 19, una proteina caratteristica delle cellule del linfoma.
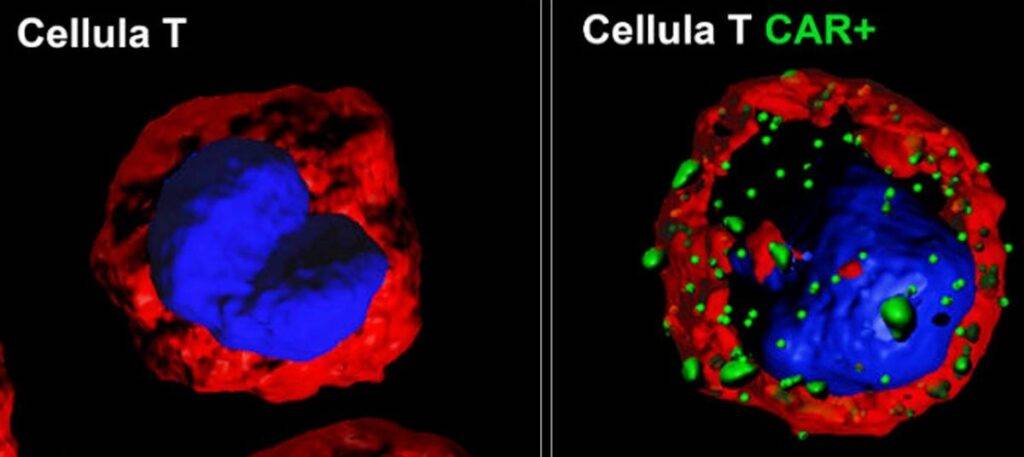
Fasi di procedura
La preparazione della terapia CAR-T richiede una procedura complessa, articolata in varie fasi:
- Prelievo: tramite un prelievo ematico si estraggono i linfociti T del paziente mediante un processo che consente di isolarli (leucaferasi).
- Ingegnerizzazione genetica: i linfociti estratti vengono modificati geneticamente mediante un virus inattivato. Tramite questo vettore virale si introduce un gene ricombinante nel linfocita, il quale permette l’espressione del recettore dell’antigene chimerico CAR sulla superficie linfocitaria. Grazie al suddetto recettore i linfociti T modificati riconoscono così un antigene specifico presente sulla superficie delle cellule tumorali, legandosi ad esso.
- Chemioterapia pre-trattamento: prima di attuare l’infusione linfocitaria, il paziente è sottoposto a chemioterapia di preparazione che permette ai linfociti T modificati di espandersi e attivarsi nell’organismo.
- Infusione: a seguito della chemioterapia di preparazione, le cellule CAR-T vengono infuse nel paziente.
- Monitoraggio: dopo l’infusione, si monitora il paziente per possibili reazioni avverse al trattamento.
Attuale utilizzo delle CAR-T
L’utilizzo delle CAR-T è stato approvato in caso di stadio avanzato di malattia, per patologie quali:
- leucemia linfoblastica acuta a cellule B, in pazienti pediatrici o giovani adulti fino a 25 anni;
- linfoma diffuso a grandi cellule B;
- linfoma primitivo del mediastino a cellule B.
Nei pazienti affetti da linfoma diffuso a grandi cellule B fino al 31% dei pazienti mantiene una remissione completa dalla malattia a 5 anni dal trattamento. Nei pazienti giovani affetti da leucemia linfoblastica tale trattamento permette di raggiungere una sopravvivenza di circa 70 mesi, se associato a ulteriori terapie cellulari (quali il trapianto allogenico). Nonostante il successo nelle neoplasie ematologiche, il panorama del trattamento della terapia con cellule T del recettore dell’antigene chimerico (CAR) per i tumori solidi è limitato.
Attualmente i pazienti pediatrici con leucemia linfoblastica acuta a cellule B trattati in prima linea con protocolli polichemioterapici hanno probabilità di guarigione anche superiori all’85% e circa il 60-70% dei pazienti con linfoma non Hodgkin di tipo DLBCL o PMBCL può ottenere un controllo di malattia a lungo termine (o guarigione) con gli attuali protocolli immunochemioterapici di prima linea, seguiti o meno da radioterapia.
Efficacia e rischi del trattamento
Rispetto alle comuni terapie in uso, le CAR-T permettono di ottenere remissioni complete anche in fasi di malattia avanzata. In vari studi clinici effettuati ai fini dell’Autorizzazione all’Immissione in Commercio (AIC) della suddetta terapia, per la leucemia linfoblastica acuta (LLA) a cellule B refrattaria, in recidiva post-trapianto, si osservano vari dati di efficacia. L’81% dei pazienti che ha ricevuto la terapia CAR-T ha ottenuto una remissione completa della leucemia; circa l’80% dei pazienti che ha ottenuto una remissione completa di malattia era ancora libero da malattia 6 mesi dopo l’infusione della terapia CAR-T; infine il 76% dei pazienti che ha ricevuto la terapia CAR-T era ancora in vita a distanza di un anno dal trattamento.
Tuttavia l’utilizzo di terapie CAR-T in alcuni casi si associa al rischio di eventi avversi, come la Sindrome da rilascio di citochine. Questa è caratterizzata da febbre, abbassamento della pressione arteriosa, aumento della frequenza cardiaca e riduzione di ossigeno nel sangue a causa dell’intensa risposta infiammatoria che si sviluppa a seguito delle CAR-T nell’organismo. Un altro evento avverso è la riduzione dei linfociti B e degli anticorpi, poiché la terapia CAR-T determina la distruzione dei linfociti B con riduzione dei livelli di anticorpi nel sangue. Anche le reazioni avverse neurologiche non sono da sottovalutare: le più osservate sono encefalopatia, afasia, delirio.
Anna Maria Musto
Fonti
- Changsong Qi, Jifang Gong, Lin Shen “Claudin18.2-specific CAR T cells in gastrointestinal cancers: phase 1 trial interim results“, Nature Medicine, 2022
- https://www.nejm.org/doi/10.1056/NEJMc2030164?url_ver=Z39.88-2003&rfr_id=ori:rid:crossref.org&rfr_dat=cr_pub%20%200pubmed