Gli aminoglicosidi rappresentano una famiglia di farmaci antibatterici dotati di elevatissima efficacia e caratterizzati da una potente azione battericida: nel corso degli anni la sintesi di nuovi composti ha radicalmente diminuito l’incidenza di effetti collaterali che in passato ne aveva limitato l’utilizzo. Impiegati di preferenza in ambito ospedaliero in occasione di infezioni gravi e spesso in associazione con gli antibiotici betalattamici, per l’elevato sinergismo; le molecole più recenti, per la loro efficacia e sicurezza, trovano comunque largo impiego anche nella pratica extra-ospedaliera.
Generalità sugli Aminoglicosidi
Gruppo piuttosto numeroso, sono dotati di struttura chimica simile, essendo costituiti da aminozuccheri uniti con legame glucosidico ad un nucleo aminociclitolo (Fig.1). ll primo amminoglicoside descritto, la streptomicina, fruttò al suo scopritore, l’ucraino Selman Abraham Waksman, il Premio Nobel per la medicina nel 1952.
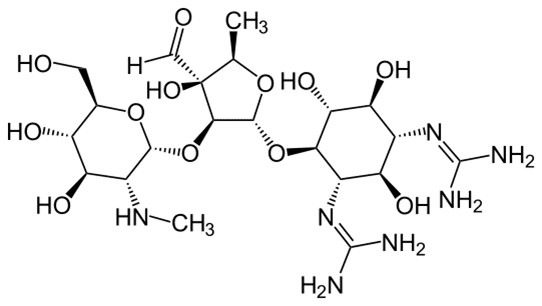
Indicazioni e controindicazioni sugli Aminoglicosidi
Gli aminoglicosidi, come anticipato, sono utilizzati maggiormente nel trattamento delle infezioni nosocomiali; le indicazioni principali sono:
- trattamento delle sepsi e delle endocarditi da: bacilli Gram negativi, streptococchi, enterococchi;
- trattamento delle infezioni da: Pseudomonas e Acinetobacter;
- sepsi di origine urinaria (per le infezioni urinarie non complicate è opportuno ricorrere a farmaci meno tossici);
- infezioni polmonari nosocomiali da Gram negativi;
- profilassi e terapia delle infezioni in chirurgia addominale e pelvica causate da flora mista.
Gravidanza e allattamento
Con gli aminoglicosidi, vi è evidenza di rischio per il feto (p. es., tossicità uditiva), ma i benefici clinici possono superare il rischio, se un aminoglicoside viene usato durante la gravidanza o se la paziente rimane incinta mentre assume uno di questi farmaci, deve essere informata del potenziale pericolo per il feto. Essi passano nel latte materno, ma non vengono ben assorbiti per via orale, il loro utilizzo è, pertanto, ritenuto compatibile con l’allattamento.
Meccanismo d’azione degli Aminoglicosidi
Gli aminoglicosidi determinano un’inibizione della sintesi proteica batterica per azione diretta sui ribosomi dei batteri mediante fissazione sulla proteina S12 della subunità 30S o su siti differenti posti tra la 30 e la 50S, con formazione di peptidi aberranti non funzionali. Legandosi alla subunità ribosomiale provocano una variazione conformazionale a carico di due basi note con passaggio syn-anti, con incapacità di corretta lettura del codice e introduzione di aminoacidi anomali. L’accumulo di proteine non funzionali danneggia le membrane cellulari causando l’espulsione di ioni K e di aminoacidi con lisi cellulare; gli aminoglicosidi attraversano la membrana batterica con un processo attivo che richiede ossigeno, i microrganismi anaerobi, quindi, risultano resistenti.
Principi attivi e farmaco cinetica
Gli aminoglicosidi possono essere classificati in base all’ origine:
- Derivati dallo Streptomyces: Streptomicina – Neomicina – Kanamicina – Tobramicina – Paromomicina – Spectinomicina
- Derivati da una micromonospora: Sisomicina – Gentamicina – Netilmicina
Sono dotati di Alta idrofilia e idrosolubilità.
Gli aminoglicosidi vengono scarsamente assorbiti per via orale dalla mucosa gastrica, pertanto, nelle infezioni sistemiche, sono impiegati per via parenterale (intravenosa e intramuscolare); vengono escreti nell’urina in forma inalterata. Essi hanno tutti la stessa emivita plasmatica di 2-3 h, che risulta notevolmente prolungata in caso di insufficienza renale; non raggiungono il SNC in quanto molecole polari.
Reazioni avverse ed interazioni
Tutti gli aminoglicosidi causano:
- Tossicità renale (spesso reversibile);
- Tossicità vestibolare e uditiva (spesso irreversibile);
- Prolungamento degli effetti dei bloccanti neuromuscolari.
I sintomi e i segni di danno vestibolare sono vertigini, e atassia.
I fattori di rischio per la tossicità renale, vestibolare e uditiva sono:
- Dosi frequenti o molto alte;
- Livelli ematici del farmaco molto elevati;
- Lunga durata della terapia (in particolare > 3 giorni);
- Età avanzata;
- Malattia renale preesistente;
- Co-somministrazione di vancomicina, agenti di contrasto iodati o altre nefrotossine;
- Per la tossicità uditiva, una predisposizione genetica, preesistenti problemi di udito e di somministrazione concomitante di diuretici dell’ansa.
E’ stata dimostrata una allergenicità crociata fra aminoglicosidi.
E’ stato riferito un aumento della nefrotossicità a seguito della somministrazione susseguente o contemporanea di altre sostanze potenzialmente nefrotossiche, quali:
cisplatino, polimixina B, colistina, streptomicina, vancomicina, kanamicina, amicacina, neomicina, paramomicina, tobramicina, organoplatini, metotrexate, alcuni farmaci antivirali (aciclovir, ganciclovir, adefovir, cidofovir, tenovir), amfotericina B, immunosoppressori quali ciclosporina.
L’uso contemporaneo con diuretici potenti quali acido etacrinico o furosemide deve essere vietato, considerato che tali diuretici posseggono una propria ototossicità e aumento la nefrotossicità.
Prove in vitro hanno evidenziato che la miscela di un aminoglicoside con antibiotici betalattamici (penicilline o cefalosporine) può comportare un’attivazione reciproca.
Meccanismi di resistenza
Finora sono stati identificati tre tipi principali di meccanismi di resistenza contro questi antibiotici:
- ridotta penetrazione dell’antibiotico; essendo idrosolubile per poter attraversare le membrane necessita di trasporto attivo con purine e ATP, meccanismo bloccato da: cationi bivalenti (calcio e magnesio), iperosmolarità, pH eccessivamente acido, anaerobiosi;
- modificazione enzimatica dell’aminoglicoside stesso a opera di enzimi batterici (transferasi) mediante adenilazione, acetilazione o fosforilazione;
- mutazione del sito legante il ribosoma.
Dr. Giosuè Ruggiano
Fonti
- Antibiotici Aminoglicosidi e classificazione | ANAP Confartigianato
- AMINOGLICOSIDI (libero.it)
- Amminoglicosidi – Wikipedia
- Aminoglicosidi (infettive.com)
- Aminoglicosidi – Malattie infettive – Manuali MSD Edizione Professionisti (msdmanuals.com)
- Figura 1: “Solfato di streptomicina”: istruzioni per l’uso, analoghi e recensioni (nextews.com)
- Immagine iniziale: Benessere in pillole: il mercato degli integratori continua a crescere (inpharmamag.it)