Che cos’è l’epigenetica?
Siamo abituati a pensare che tutte le modificazioni fenotipiche e tutto ciò che riguarda l’ereditabilità, sia una prerogativa del DNA. In effetti, il DNA contiene tutte le informazioni per la produzione di proteine (e non solo), eppure il semplice codice genetico non basta per l’espressione dell’informazione. A questo punto entra in gioco l’epigenetica, ossia la scienza che studia le modificazioni ereditabili che variano l’espressione genica, pur non alterando la sequenza nucleotidica del DNA. Andiamo però con ordine e vediamo cosa riguarda questa definizione.
Abbiamo, quindi, detto che l’espressione genica, e dunque la produzione di molecole quali le proteine, non dipendono esclusivamente dal codice genetico. Un altro fattore che concorre a questa produzione è la struttura della cromatina. A seconda infatti della sua struttura, se rilassata o impacchettata, si possono attivare o silenziare i geni. Modificazioni riguardanti questo grado di compattamento risultano ereditabili e hanno, ovviamente, effetti sul fenotipo.
Anche il grado di metilazione del DNA sembrerebbe essere correlato al controllo dell’espressione genica ed è anche il processo alla base dell’imprinting genomico.
I meccanismi principali epigenetici sono due:
- Rimodellamento della cromatina;
- Metilazione del DNA.
La cromatina
Prima di vedere i meccanismi, è bene fare un ripasso su cosa sia la cromatina.
Il DNA all’interno della cellula è finemente organizzato in una serie di livelli, primo tra questi la fibra cromatina. La cromatina è la risultante dell’interazione tra DNA e istoni, ovvero proteine basiche su cui il DNA si avvolge. La struttura che si forma si può paragonare, nella sua forma meno condensata, ad una collana di perle (Figura 1), in cui ogni perla è chiamata nucleosoma. Ogni nucleosoma è formato da otto proteine istoniche, due per ogni tipo, e da un tratto di DNA. Per finire, esiste un quinto istone che si lega al DNA in uscita dall’ottamero istonico. Questo legame è particolarmente importante ai fini della compattazione, in quanto devia l’angolo di uscita del DNA.

L’epigenetica e il rimodellamento della cromatina
Il rimodellamento della cromatina è un processo che permette di cambiare la conformazione della cromatina con conseguente espressione o silenziamento dei geni. Questi tipi di cambiamenti sono trasmessi da una cellula madre a una cellula figlia. Ci sono tre modi per modellare la cromatina: modificare gli istoni, utilizzare i complessi di rimodellamento della cromatina e sostituire gli istoni con delle loro varianti.
Modificazione degli istoni
Nel primo caso gli istoni subiscono modificazioni chimiche a livello della loro estremità N-terminale, che fuoriesce dal nucleosoma. Tra le diverse modificazioni abbiamo la metilazione, l’acetilazione e la fosforilazione.
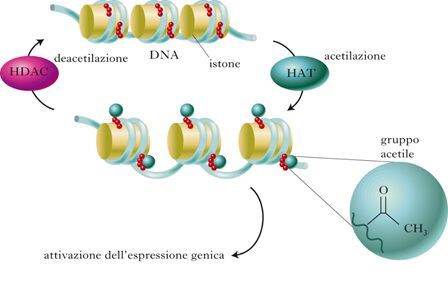
L’acetilazione (Figura 2), in particolare, è generalmente un evento associato all’attivazione trascrizionale. L’aggiunta di un gruppo acetile a residui di lisina porta infatti ad una riduzione della carica negativa degli istoni con conseguente rilassamento della cromatina. Una cromatina maggiormente rilassata sarà dunque più facilmente attaccabile dai fattori della trascrizione.
Complessi di rimodellamento della cromatina
I complessi di rimodellamento della cromatina sono una famiglia di proteine che, agendo a livello dei nucleosomi, rendono accessibili tratti di DNA ai fattori trascrizionali, permettendo quindi l’espressione genica. A reclutare questi complessi ci sono dei fattori specifici capaci di riconoscere le giuste sequenze. Una volta arrivato il rimodellatore, esso idrolizza ATP per modificare la struttura della cromatina.
Tra i diversi complessi di rimodellamento ci sono SWI/SNF e ISWI. I primi generalmente aprono la struttura della cromatina ed attivano l’espressione genetica, mentre, del secondo gruppo, fanno parte i complessi che reprimono la trascrizione.
Varianti degli istoni
Infine, esistono alcune varianti delle proteine istoniche che, se sostituite a quelle “originali”, provocano un alterata interazione tra ottamero e DNA. L’esistenza di queste varianti riguarda soprattutto gli istoni più accessibili e quindi, anche, più sostituibili. Proteine come H4 infatti non dispongono di nessuna variante, mentre esistono quattro forme diverse per H3
L’epigenetica e la metilazione del DNA
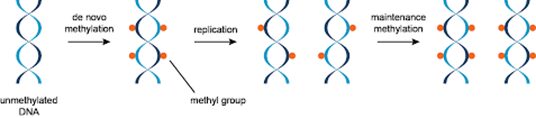
Un altro meccanismo epigenetico consiste nella metilazione del DNA e in particolare nella metilazione della citosina. Le citosine metilate sono principalmente quelle facenti parti delle isole CpG, ovvero quelle che sono seguite da una guanina (la “p” indica invece il gruppo fosfato). Il processo di metilazione del DNA (Figura 3) avviene per mezzo di enzimi, chiamati DNA metiltransferasi (DNMT). Tra questi abbiamo le “metilasi de novo” (DNMT3A e DNMT3B), che hanno il compito di aggiungere nuovi gruppi metilici a specifiche sequenze cromosomiche. Dopodiché, a seguito della replicazione, i siti emimetilati (senza metile) vengono metilati da enzimi, chiamati “metilasi di mantenimento” (DNMT1).
Ma cosa ha a che fare tutto questo con l’epigenetica? La metilazione di queste regioni ha un ruolo nell’attivazione o nello spegnimento dei geni. Si è visto infatti che l’ipermetilazione nella regione del promotore di un gene porta all’inibizione della trascrizione. Al contrario l’ipometilazione è correlata all’attivazione trascrizionale. In poche parole, la presenza di citosine metilate porterebbe al silenziamento dei geni.
Di nuovo quindi, siamo davanti ad una modificazione che, pur non riguardando una variazione della sequenza nucleotidica del DNA, porta ad un controllo dell’espressione genetica.
Imprinting genomico
La metilazione delle citosine è anche alla base di un processo che va sotto il nome di imprinting genomico. Nell’imprinting genomico solo uno dei due geni omologhi viene espresso mentre l’altro viene silenziato, tramite metilazione. Presi quindi due cromosomi omologhi, di cui uno di origine materna e uno di origine paterna, alcuni geni espressi saranno esclusivamente provenienti o dalla madre o dal padre.
Si conoscono inoltre malattie genetiche correlate al fenomeno dell’imprinting. Ci sono, infatti, malattie dovute ad una assenza di proteina (perdita allele non soggetto a imprinting) o malattie in cui la concentrazione di proteina viene raddoppiata (perdita dell’imprinting).
Fonti
- https://www.treccani.it/;
- Amaldi, F. Biologia molecolare, Zanichelli, Terza Edizione, 2018;
- Immagine in evidenza: https://www.issrgo.it/origine-dellepigenetica-umana/
- https://www.greelane.com/it/scienza-tecnologia-matematica/scienza/chromatin-373461/;
- https://www.treccani.it/enciclopedia/epigenetica_%28Dizionario-di-Medicina%29/;
- http://othes.univie.ac.at/29377/1/2013-06-18_0800602.pdf
Complimenti Chiara! Veramente un lavoro di divulgazione, completo e comprensibile, che mostra la qualità del tuo studio e l’impegno. Resta un problema di base: la semplificazione può arrivare solo fino ad un certo punto, altrimenti perde in precisione, e quindi il discorso è fruibile da chi già possiede delle nozioni scientifiche.