Un sushi di batteri, chef!
Sushi letteralmente significa riso stagionato ma non è l’unico ingrediente del cibo che da tempo è particolarmente di moda. Ad avvolgere il riso e il pesce vengono usate sempre le stesse alghe e da secoli quelle dello stesso genere, la Porphyria conosciuta ai più come alga Nori.

L’alga Porphyria
Se ne conosco ben 70 specie. Hanno molte proprietà benefiche tra cui un elevato contenuto di Omega 3 e la crescita rapida. Insomma delle super lattughe marine! Ma non è a queste loro particolarità che si è interessato lo studio del team di Mirjam Czjzek, chimico della Station Biologique de Roscoff, sulla costa della Bretagna in Francia.


Figura 2 – Foto di Porphyria in natura [Fonte: https://flickr.com/photos/kqedquest/3115931485] e foto di alga Porphyria essiccata usata nella preparazione del sushi [Fonte: https://schaechter.asmblog.org/schaechter/2010/05/you.html]
A differenza delle piante terrestri, i carboidrati che compongono le alghe sono ricoperti di molecole di zolfo, quindi sono necessari enzimi speciali per scomporli. Sappiamo che i batteri che compongono la comunità che popola il nostro intestino è indispensabile per la digestione e la preparazione dei nutrienti che poi vengono internalizzati nelle cellule intestinali.
Zobellia galactanivorans
Quindi potrebbe esistere un batterio tipico del microbioma dei giapponesi o ancora di più un batterio che abbia insegnato a digerire più efficacemente le alghe Nori alle cellule intestinali della popolazione giapponese che da secoli consuma questo alimento? La risposta esiste in un batterio marino, Zobellia galactanivorans, noto per la sua passione per le alghe Nori.
Z. galactanivorans è un batterio marino gram-negativo isolato dalla superficie delle alghe rosse della costa francese. Forma colonie gialle e ha una morfologia a bacillo o diplobacillo. E’ mesofilo e degrada sia la carragenina, un polisaccaride lineare solfato, che l’agar, entrambi presenti nella parete cellulare delle alghe rosse. Z. galactanivorans contiene il gene porB che codifica per l’enzima β-porfiranasi-B in grado di scomporre i carboidrati solfati derivati dalla digestione delle alghe rosse.
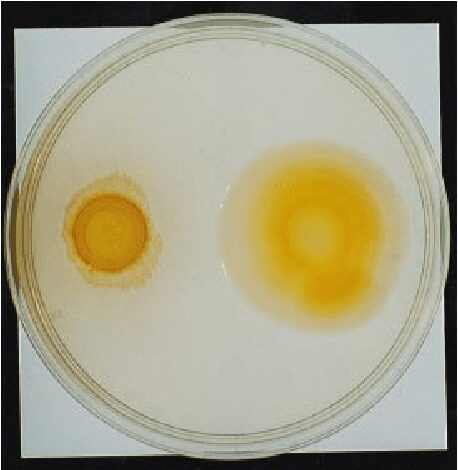
[Fonte: https://www.semanticscholar.org/paper/Zobellia-galactanovorans-gen.-nov.%2C-sp.-nov.%2C-a-of-Barbeyron-L%E2%80%99Haridon/89bc7cabb15365fb957079722e5acbc05455b905]
Microbioma giapponese vs microbioma americano
La ricerca ha portato alla luce cinque geni in Z. galactanivorans che sembravano codificare per enzimi in grado di scomporre i particolari carboidrati presenti nelle alghe marine. Quando i ricercatori hanno trasferito questi geni a un altro batterio costretto a mangiare carboidrati di alghe, hanno scoperto che due geni erano particolarmente attivi.
In particolare il batterio Bacteroides plebeius ha mostrato, dopo un’estesa analisi metagenomica per le sequenze che corrispondevano ai due geni di Z. galactonivorans, la presenza dei due geni codificanti per l’enzima utile alla perfetta digestione delle Porphyria. E sorpresa, il batterio in questione è presente solo nell’intestino di individui giapponesi. Phocaeicola plebeius, precedentemente Bacteroides plebeius, è un microbo che si trova nell’intestino umano, più spesso presente nei nativi del Giappone. P. plebeius contiene un gene noto come BACPLE_01693, codificante per la β-porfiranasi-A che idrolizza i legami dei carboidrati delle alghe rosse.

Chiedendosi poi se gli enzimi fossero unici per gli individui giapponesi, il team di Czjzek ha confrontato i genomi microbici di 13 giapponesi con quelli di 18 nordamericani. Cinque dei soggetti giapponesi avevano l’enzima, ma tra i nordamericani “non ne abbiamo trovato nemmeno uno”, afferma Czjzek.
Come i batteri mangiano per noi (e ci aiutano a digerire il sushi)
I microbi intestinali forniscono al corpo umano energia dai polisaccaridi alimentari attraverso enzimi attivi sui carboidrati, denominati CAZymes, che sono assenti nel genoma umano. Questi enzimi agiscono sui polisaccaridi delle piante terrestri che hanno dominato la dieta durante l’evoluzione umana. Esiste ad oggi un database di tutti gli enzimi geneticamente inclusi nella denominazione CAZymes, enzimi coinvolti nella degradazione dei polisaccaridi. CAZy è stata fondata nel 1999, al fine di fornire un accesso online e costantemente aggiornato alla classificazione della famiglia di CAZymes, basata sulla sequenza proteica, originariamente sviluppata all’inizio degli anni ’90 per classificare le idrolasi glicosidici. Le nuove voci vengono aggiunte poco dopo la loro comparsa nelle versioni giornaliere di GenBank.
La rapida evoluzione del sequenziamento del DNA ad alta velocità ha portato alla continua crescita esponenziale del database CAZy, che ora copre centinaia di migliaia di sequenze. CAZy continua ad essere curato e sviluppato dal gruppo Glycogenomics presso AFMB (Architecture et Fonction des Macromolecules Biologiques), un centro di ricerca affiliato al Centro nazionale francese per la ricerca scientifica e all’Università di Aix-Marseille. Questa risorsa è a disposizione della comunità scientifica da oltre 10 anni, contribuendo alla diffusione delle informazioni e fornendo una nomenclatura trasversale ai glicobiologi. Più recentemente, questa risorsa è stata utilizzata per migliorare la qualità delle previsioni funzionali di numerosi progetti sul genoma fornendo annotazioni di esperti.
Trasferimento genico
Dove potrebbero i batteri all’interno dell’intestino umano avere acquisito la capacità di produrre un enzima che digerisce le alghe? E’ stato ipotizzato che potrebbe essere avvenuto un trasferimento genico laterale, un meccanismo molto comune tra batteri, dai batteri che vivono sulle alghe a quelli intestinali.
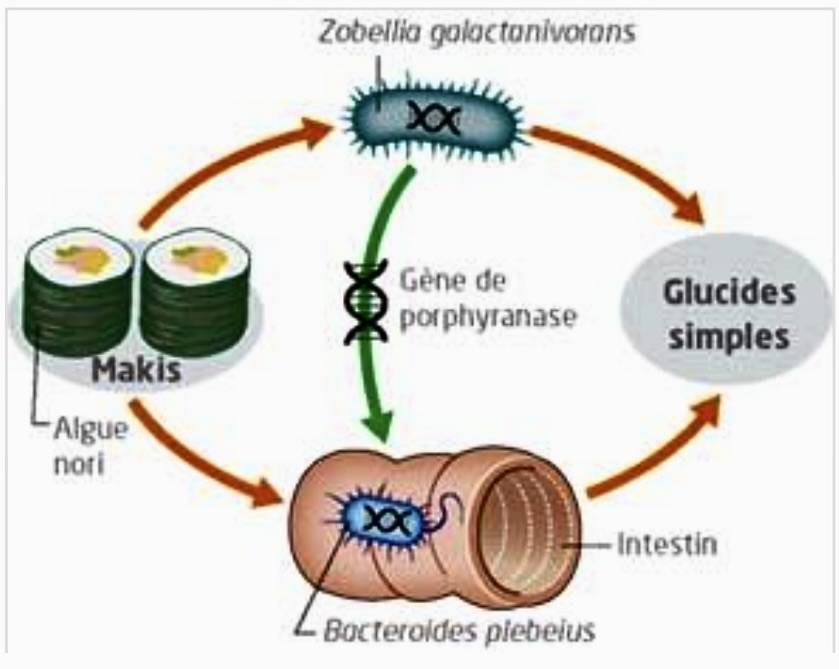
Già dai documenti fiscali risalenti all’VIII secolo d.C., le alghe erano utilizzate come forma di pagamento nella società giapponese. Il Nori, l’alga usata per avvolgere il sushi o il wakame, viene spesso servita nella zuppa di miso; consumata giorno dopo giorno, i batteri nell’intestino avrebbero avuto così la possibilità di incorporare materiale genetico dai loro cugini marini.
La capacità di “sgranocchiare” alcuni carboidrati in più potrebbe aver dato a questi batteri intestinali un vantaggio rispetto alle migliaia di concorrenti, e indirettamente favorendo la digestione del sushi.
Bibliografia
- https://www.science.org/content/article/japanese-guts-are-made-sushi
- https://www.repubblica.it/il-gusto/2022/04/06/news/sushi_poco_digeribile-344359583/
- https://www.tuttogreen.it/alga-nori-benefici-usi/amp/#Varieta_di_alga_nori_conosciute
- https://www.sb-roscoff.fr/fr/file/station-biologique-roscoff-zobellia-galactanivorans-3942jpg
- https://www.nature.com/articles/nature08937
- https://www.nature.com/articles/news.2010.169
- https://www.cell.com/cell-host-microbe/fulltext/S1931-3128(22)00087-7
- https://labblog.uofmhealth.org/lab-report/your-gut-on-sushi
- https://www.ncbi.nlm.nih.gov/pmc/articles/PMC2686590/
- http://www.cazy.org/
- https://www.microbiologiaitalia.it/alghe/pseudokirchneriella-subcapitata/
- https://www.news-medical.net/life-sciences/What-is-the-Carbohydrate-Active-Enzyme-Classification-System.aspx
- https://en.wikipedia.org/wiki/Zobellia_galactanivorans
- https://www.tuttogreen.it/alga-nori-benefici-usi/amp/#Varieta_di_alga_nori_conosciute