Il carcinoma del colon-retto (CRC) è il terzo tumore più frequente e anche la quarta causa di morte correlata al cancro in tutto il mondo. Si tratta di una malattia complessa, associata a fattori sia genetici che ambientali, come lo stile di vita e le abitudini alimentari. Da studi recenti è emersa anche una correlazione con il microbiota intestinale e con un batterio in particolare, Fusobacterium nucleatum, che non solo colonizza il carcinoma del colon in misura maggiore rispetto a quanto faccia col tessuto sano, ma è anche considerato un fattore di rischio per la progressione del CRC.
Chi è Fusobacterium nucleatum?

Il nostro pericoloso inquilino è un batterio Gram-negativo anaerobico, che in condizioni normali popola principalmente la cavità orale ed è responsabile di infiammazioni come periodontite e gengivite. Che cosa ci fa quindi nel tumore del colon?
In generale, nel micro-ambiente tumorale succedono una serie di cose che facilitano l’ingresso e la colonizzazione da parte del batterio: la creazione e aumentata permeabilità dei vasi sanguigni, la carenza di ossigeno nelle regioni interne del tumore, la soppressione della risposta immunitaria…sono il sogno di qualsiasi microrganismo anaerobico in cerca di una casa! Ma esiste anche un fattore specifico: il tumore esprime un polisaccaride (Gal-GalNAc) che viene riconosciuto e legato da una proteina di Fusobacterium, la lectina Fap2. Grazie a questo sistema di riconoscimento, Fusobacterium riesce persino a localizzare e colonizzare le metastasi.
Come si comporta Fusobacterium dentro il tumore?
Purtroppo, il batterio non se ne sta tranquillo e per i fatti suoi, ma partecipa attivamente alla progressione tumorale e secondo recenti studi anche alla sua nascita. Esso genera infatti un contesto infiammatorio che aumenta l’aggressività del tumore, la proliferazione cellulare e la disseminazione delle metastasi. Come se non bastasse, la lectina Fap2 blocca anche l’azione citotossica delle NK e linfociti T contro le cellule tumorali, proteggendole dagli attacchi del sistema immunitario. Non sorprende quindi che la presenza di questo batterio correli con una prognosi peggiore, una aumentata probabilità di ricadute e di esito fatale della malattia.
F. nucleatum è anche probabilmente responsabile della resistenza alla chemioterapia, uno degli ostacoli maggiori contro cui si misurano i medici che curano questo tipo di tumore. Il CRC viene normalmente trattato con farmaci chemioterapici come il 5-fluoruracile (5-FU), che interferisce con la replicazione del DNA. Purtroppo, la maggioranza dei pazienti con CRC in stadio avanzato risponde inizialmente alla terapia, ma è soggetta a frequenti ricadute causate dalla resistenza al farmaco e meno del 10% è ancora vivo a 5 anni dalla diagnosi. Non disponiamo ancora di metodi veramente efficaci per curare questi pazienti ed è quindi fondamentale comprendere e contrastare i meccanismi della chemioresistenza. Nei pazienti con ricadute post-chemioterapia, la frequenza di F. nucleatum è maggiore e una recente ricerca ha dimostrato il ruolo critico di questo batterio.
Altre informazioni
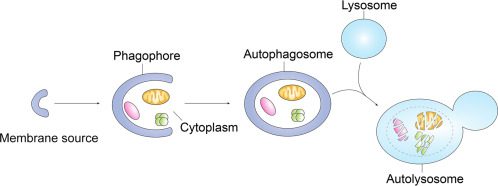
Gli scienziati sono riusciti a ricostruire la complessa rete di componenti che vengono modulati quando Fusobacterium entra nella cellula. Essa comprende i micro-RNA e i complessi molecolari responsabili dell’autofagia. I primi sono piccoli filamenti di RNA che regolano l’espressione di determinati geni: la presenza del batterio causa una perdita dei micro-RNA che bloccano la via di segnalazione autofagica. L’autofagia, invece, è un processo di riciclo di componenti cellulari che è stato spesso correlato con la resistenza alla chemioterapia: in condizioni di stress, la cellula sopravvive “nutrendosi” delle proteine in eccesso o non necessarie e degli organelli danneggiati. Quindi, riassumendo, i ricercatori hanno dimostrato che Fusobacterium modula la chemioresistenza del tumore al colon “schiacciando l’interruttore” dell’autofagia.
Tutti questi studi suggeriscono che è fondamentale monitorare la frequenza di F. nucleatum nei pazienti con CRC per la diagnosi e soprattutto la prognosi della malattia, ma sottolineano anche la necessità di terapie alternative per il tumore del colon, che potrebbero combinare la tradizionale chemioterapia con farmaci anti-Fusobacterium o persino con inibitori dell’autofagia. Una strategia ancora più visionaria è quella di trasformare Fusobacterium da nemico…ad alleato!
Come si dice: se non puoi sconfiggere il tuo nemico, fattelo amico: vista la sua capacità di raggiungere il tumore, un’ipotesi potrebbe essere quella di ingegnerizzare il batterio, trasformandolo in una piattaforma per veicolare trattamenti di tipo chemioterapico o immunoterapico direttamente nelle cellule tumorali.
Erika Salvatori
Fonti:
- Abed, J., et al. (2017). Tumor Targeting by Fusobacterium nucleatum: A Pilot Study and Future Perspectives. Front. Cell. Infect. Microbiol.
- Yu, TaChung et al. (2017). Fusobacterium nucleatum Promotes Chemoresistance to Colorectal Cancer by Modulating Autophagy. Cell.
- Fu-Mei Shang and Hong-Li Liu (2018). Fusobacterium nucleatum and colorectal cancer: A review. World J. Gastrontest. Oncol. 10(3): 71–81.