Italia al primo posto per Antibiotico-resistenza
Antibiotici: A che farmaci pensiamo in primis come prescrittori? Amoxicillina/acido clavulanico e ciprofloxacina probabilmente. Eppure, per la maggior parte delle comuni infezioni, dalla tonsillite alla cistite, le suddette molecole hanno uno spettro d’azione inutilmente ampio.
Discorso a parte invece per l’ampia quota di affezioni – più o meno – chiaramente virali, per cui il paziente chiede l’antibiotico “di rinforzo” e a cui non si riesce a dire di no.
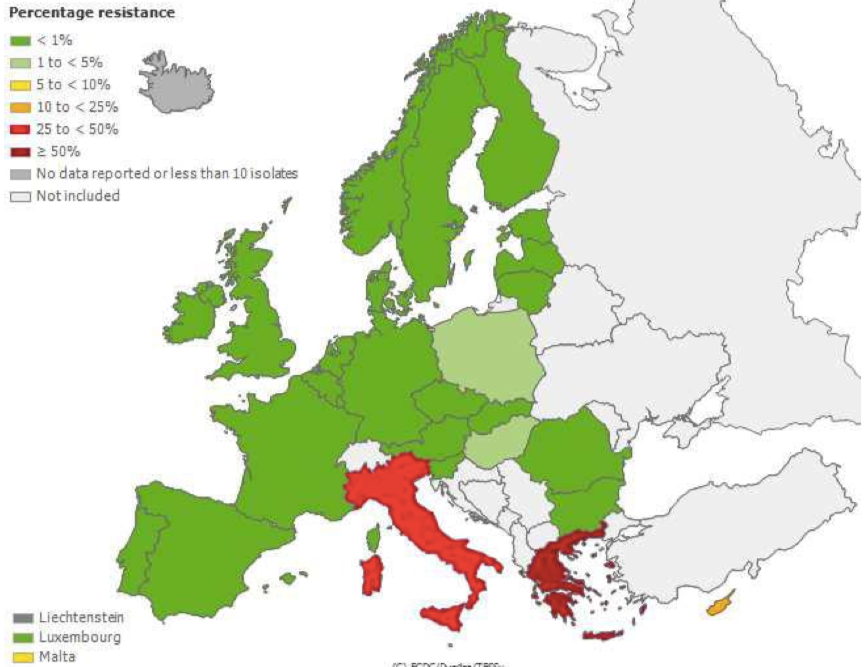
L’Italia è prima in Europa per anni di salute persi e per morti a causa di germi multiresistenti e figura tra i paesi con percentuali più elevate di ceppi multiresistenti tra gli isolati di Staphylococcus aureus, enterococchi, Escherichia coli, Klebsiella pneumoniae, Pseudomonas aeruginosa e Acinetobacter baumannii.
Tra le cause di questo vi sono sicuramente l’uso generoso di antibiotici, sia a livello umano che veterinario, la facile scelta da parte del personale medico di preparati ad ampio spettro rispetto a terapie mirate e a spettro ristretto, la non corretta implementazione a tutti i livelli di pratiche finalizzate alla prevenzione delle infezioni correlate all’assistenza (es: cateteri vescicali, lesioni da decubito, ecc). E’ chiaro anche che si instaura un circolo vizioso, in cui più resistenti sono i germi, più ad ampio spettro diventano le terapie empiriche, e così via.
Probabilmente il contenzioso medico-legale, particolarmente vivace nel nostro paese, gioca un ruolo nel far pendere il piatto della bilancia più facilmente verso la prescrizione di un antibiotico.
Variabilità regionale nel consumo di antibiotici
In Italia vi è una evidente variabilità regionale nel consumo di antibiotici, con consumi più sostenuti a Sud, macroregione che presenta consumi nettamente superiori rispetto alla media europea (prima la Campania con 24.7 Daily Defined Doses/1000 abitanti/die, ultima la Provincia Autonoma di Bolzano con 11.2. Media europea: 20.1 DDD/1000 abitanti/die).
Nel 2017 il Ministero della Salute ha pubblicato il Piano Nazionale di Contrasto dell’Antimicrobico-Resistenza (PNCAR) con chiare indicazioni e strategie a livello medico (umano), veterinario, di ricerca e di sensibilizzazione dell’opinione pubblica.
Global Action Plan on Antimicrobial Resistance
L’OMS definisce l’antibiotico-resistenza come una delle minacce più serie alla salute globale, alla sicurezza alimentare e allo sviluppo e ha pubblicato nel 2015 il Global Action Plan on Antimicrobial Resistance con un elenco di obiettivi strategici che spaziano dalla popolazione generale alla ricerca su nuovi farmaci.
Un contrasto efficace all’incremento dei livelli di antibiotico-resistenza si basa, tra le altre cose, su:
- continua formazione e aggiornamento del personale sanitario con focus sulle linee guida;
- non trattamento indiscriminato di condizioni quali bronchite acuta, batteriuria asintomatica negli anziani, ecc;
- istituzione di enti locali di antimicrobial stewardship;
- digitalizzazione delle cartelle cliniche, che consente la registrazione e visualizzazione rapida dello stato di portatore di germe multiresistente;
- mantenimento di buone pratiche di igiene per la prevenzione delle infezioni correlate all’assistenza;
- educazione sanitaria della popolazione, per evitare il fenomeno di richiesta inappropriata di antibiotici.
Tutto questo alla luce anche della stima condotta dalla Commissione Europea sui costi dell’antimicrobial resistance: 1 miliardo e mezzo di euro l’anno, destinati a crescere con l’aumento dei livelli di resistenza. Uscite che gravano e graveranno sulla già appesantita spesa pubblica italiana.
Fonti
- [1] M. De Martino et. al. “Linee Guida Italiane. Gestione della Faringotonsillite in Età Pediatrica”
- [2] Raccomandazioni in tema di diagnosi, trattamento e profilassi delle infezioni delle vie urinarie, Società Italiana di Urologia, 2015.
- [3] Cassini A. et al. “Attributable Deaths and Disability-Adjusted Life-Years Caused by Infections with Antibiotic-Resistant Bacteria in the EU and the European Economic Area in 2015: a Population-Level Modelling Analysis.” The Lancet Infectious Diseases, vol. 19, no. 1, 2019, pp. 56–66., doi:10.1016/s1473-3099(18)30605-4.
- [4] European Centre for Disease Prevention and Control. Surveillance of antimicrobial resistance in Europe 2018. Stockholm: ECDC; 2019
- [5] Tebano G. et al. “ESCMID Study Group for Antimicrobial stewardshiP (ESGAP), Defensive medicine among antibiotic stewards: the international ESCMID AntibioLegalMap survey.” Journal of Antimicrobial Chemotherapy, Volume 73, Issue 7, July 2018, Pages 1989–1996, https://doi.org/10.1093/jac/dky098
- [6] Osservatorio Nazionale sull’impiego dei Medicinali. L’uso degli antibiotici in Italia. Rapporto Nazionale 2017. Roma: Agenzia Italiana del Farmaco, 2019
- [7] European Centre for Disease Prevention and Control. Antimicrobial consumption in the EU/EEA, annual epidemiological report for 2018. Stockholm: ECDC; 2019.
- [8] Piano Nazionale di Contrasto dell’Antimicrobico-Resistenza (PNCAR) 2017-2020
- [9] Global Action Plan on Antimicrobial Resistance. World Health Organization 2015. ISBN 978 92 4 150976 3
- [10] https://ec.europa.eu/health/amr/sites/health/files/antimicrobial_resistance
La figura 2 si riferisce alla resistenza di Klebsiella pneumoniae