Caratteristiche
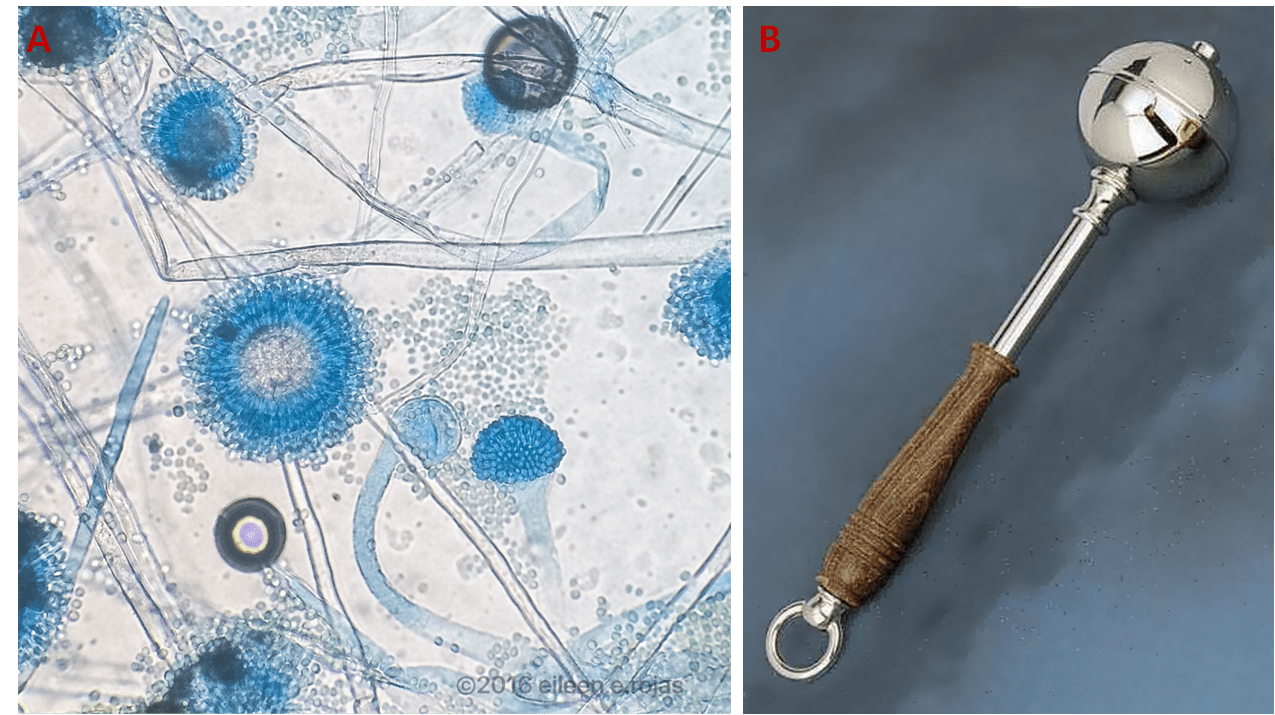
Il micete Aspergillus niger (Fig. 1A) è una muffa appartenente al phylum degli Ascomiceti, raffigura l’agente eziologico della “muffa nera” su alcuni frutti e verdure, tra cui uva, albicocche, cipolle, aglio e arachidi, ed è un contaminante abituale dei cibi. Il nome ha origine dalla parola latina “aspèrges”, che designa l’aspersorio, cioè lo strumento che i preti usano per spargere l’acqua santa sul popolo (Fig. 1B). Nel 1729 il botanico italiano Pier Antonio Micheli studiò in maniera meticolosa questi microorganismi e descrisse la struttura “ad aspersorio” dell’Aspergillus, introducendo quindi un nuovo genere di miceti che ancora ai giorni nostri è riconosciuto come tale.
Come gli altri funghi del genere Aspergillus, A. niger è cosmopolita, ubiquitario, si può riscontrare nel terreno, nei materiali organici vegetali e animali, e rilascia una mole apprezzabile di tossine, la cui tossicità dipende dal genotipo (alcuni ceppi producono le ocratossine, che sono nefrotossiche e possono promuovere i tumori renali. Tra queste abbiamo l’ocratossina A, dalla quale si formano l’ocratossina B, per declorazione, e l’ocratossina C, per esterificazione). In aggiunta a ciò, questo fungo prolifera su substrati caratterizzati da abbondanti quantità di polisaccaridi (come l’amilosio) e di carbonio (per esempio i monosaccaridi come il glucosio, il galattosio, il mannosio); non a caso gli alimenti contenenti alte concentrazioni di amido (patate e cereali) rappresentano le riserve migliori per la crescita del micete. Comunque, le muffe del genere Aspergillus riescono a moltiplicarsi anche senza la necessità di nutrienti; l’A. niger è un esempio, in quanto attecchisce senza problemi sulle pareti umide.
Le spore (o conidi) secrete da A. niger si propagano mediante l’aria e vengono inalate in quantità apprezzabile dagli esseri umani (in particolare nel luoghi chiusi o nelle aree distinte da una vegetazione rigogliosa), anche se raramente l’esposizione alle spore è causa di malattie. Infatti l’Aspergillus non è classificato come un fungo patogeno al 100%, dal momento che negli individui sani non ha alcun effetto avverso (al contrario nelle persone con un sistema immunitario indebolito o affette da alcune malattie genetiche può causare un’infezione chiamata aspergillosi, di cui parleremo più avanti). In ogni caso, è prevalentemente un componente della flora commensale umana e un saprofita che vive sulla vegetazione in decomposizione e sulle foglie morte. Ciononostante, si comporta come un parassita degli uccelli, nei quali è responsabile di infezioni polmonari anche fatali, e provochi aborto nei bovini e negli ovini.
C’è da dire che A. niger tollera elevate temperature (termotollerante), ha un intervallo di crescita tra 10 °C e 40 °C, e la temperatura ideale per germogliare è di 31 °C. Molto interessante è uno studio recente, effettuato sulla Stazione Spaziale Internazionale e pubblicato su Frontiers of Microbiology, in cui si rivelò che A. niger è estremamente resistente alle radiazioni spaziali, tra cui raggi ultravioletti, raggi X e radiazioni cosmiche. In questo esperimento le spore vennero esposte a dosi di radiazioni fino a 1000 Gy e 4000 J/m₂ scoprendo che questo micete è dotato di una robustezza notevolmente maggiore rispetto ad altri microorganismi radio-resistenti (per esempio il batterio Deinococcus radiodurans).
Filogenesi
Dominio Eukaryota
Regno Fungi
Phylum Ascomycota
Subphylum Pezizomycotina
Classe Eurotiomycetes
Sottoclasse Eurotiomycetidae
Ordine Eurotiales
Famiglia Trichomonaceae
Genere Asperigillus
Specie A. niger
Morfologia
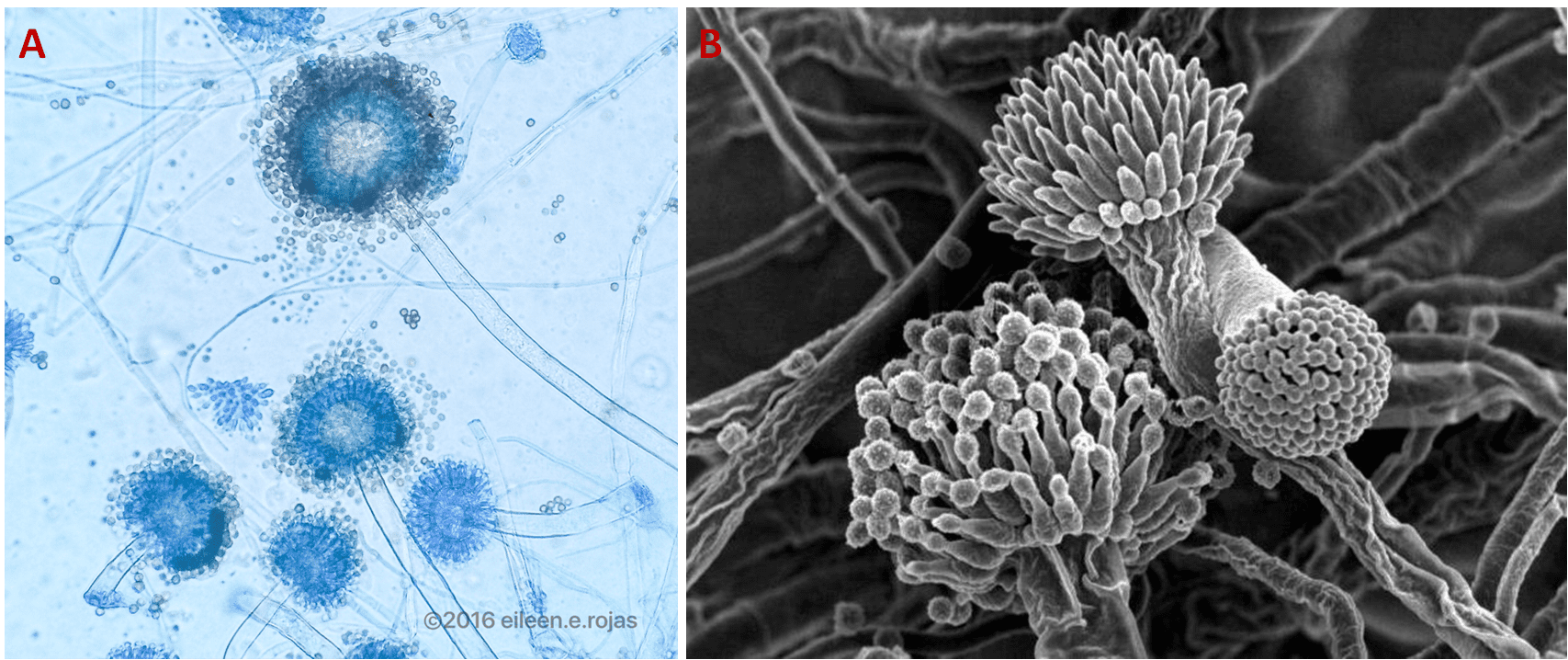
A livello microscopico, A. niger è contraddistinto da teste a disposizione radiata che tendono a suddividersi in colonne (Fig. 3B). I componenti primari del micete sono le ife filamentose che ricordano delle piccole piante, i conidi (spore asessuate) e i conidiofori (protrusioni delle ife da cui nascono i conidi). I conidi appaiono globosi, ovali, dalla superficie rugosa con creste e spigoli, neri o bruni (Fig. 3A e 3B). I conidiofori sono lunghi da 400 a 3000 μm, hanno una superficie ialina e liscia, sono incolori, bruni nella zona apicale, e terminano con dei rigonfiamenti, le vescicole (Fig. 3A e 3B). Queste producono delle cellule ialine o scure chiamate metule, le quali hanno la funzione di supportare le fialidi (Fig. 2); il termine “fialide” indica la cellula terminale del conidioforo oppure il conidioforo stesso sulla cui sommità sono posizionati i conidi, che in tal caso si definiscono fialospore. Le fialidi presentano una texture irregolare, sono marroni scuro e hanno un diametro di 4-5 μm.

Dal punto di vista macroscopico A. niger di solito esibisce un aspetto cotonoso, al principio le colonie vanno dal biancastro al giallastro e in seguito virano al nero (che coincide con la testa del micete), hanno dei margini asimmetrici di colore giallo pallido che producono fessure radiali. Queste caratteristiche si possono osservare facendo crescere il micete sul terreno Potato Dextrose Agar (PDA) alla temperatura di 25 °C (Fig. 4A e 4B).
Sull’agar estratto di malto (MEA), previa incubazione di sette giorni a 25 °C e 37 °C, si formano delle colonie leggermente marroni con gruppi di conidi dall’aspetto levigato (Fig. 4C e 4D).
Infine sul Czapek Yeast Agar (CYA), dopo cinque giorni di incubazione a 25 °C e 37 °C, si sviluppano delle colonie nere con un insieme di conidi dalla superficie lanosa (Fig. 4E e 4F).

Patogenesi
L’infezione da A. niger, ma anche dalle altre specie (A. fumigatus, A. flavus), viene chiamata aspergillosi, che colpisce l’apparato respiratorio (i polmoni) e raffigura un’infezione opportunistica, ovvero che si manifesta specialmente in individui con un sistema immunitario indebolito (affetti da AIDS, in terapia immunosoppressiva per ricevere un trapianto d’organo o di midollo osseo, in terapia prolungata e ad alte dosi con corticosteroidi, malati di leucemia). Di rado coinvolge individui immunocompetenti. Non dobbiamo dimenticare che l’Aspergillus è un microorganismo commensale della cute, della cavità orale e dell’apparato digerente.
A. niger e A. fumigatus rappresentano le specie maggiormente implicate nell’aspergillosi, le cui forme più frequenti ed importanti sono tre:
- Aspergillosi bronco-polmonare allergica, che riguarda individui che soffrono d’asma o affetti da fibrosi cistica (una malattia genetica causata dalla mutazione di un canale del cloro che provoca gravi problemi respiratori a causa del ristagno di muco denso nei bronchi). Ѐ connessa a una reazione aggressiva di ipersensibilità stimolata dall’inalazione delle spore del micete, ed è caratterizzata da asma con infiltrati di cellule immunitarie che possono indurre broncopolmonite con fibrosi dei segmenti polmonari, dispnea intensa, bronchiectasie (dilatazioni irreversibili dei bronchi), malessere e tosse. In seguito al contatto tra gli allergeni e le immunoglobuline di tipo E (IgE), vengono attivati i mastociti (globuli bianchi coinvolti nelle allergie, rappresentano l’equivalente dei basofili ma sono localizzati nei tessuti connettivi propriamente detti e non nel sangue), i quali producono istamina (una molecola di segnale generata dalla decarbossilazione dell’istidina che agisce da potente vasodilatatore e bronco-costrittore) con conseguente broncospasmo e rilascio di muco nei bronchioli;
- Aspergillosi locale non invasiva, che è distinta dall’assenza di invasione dei tessuti limitrofi e si suddivide in aspergilloma, otomicosi, onicomicosi, infezioni oculari e aspergillosi cutanea primaria. Nella prima si verifica la creazione di ife fungine all’interno di cavità preesistenti nel parenchima polmonare in seguito a tubercolosi e sarcoidosi (malattia infiammatoria che interessa di solito i polmoni e i linfonodi mediastinici). Questa malattia al principio è asintomatica per poi evidenziarsi con tosse cronica, emottisi (a causa delle lesioni dei vasi sanguigni adiacenti alla cavità), fiacchezza, inappetenza e anoressia. La seconda, che colpisce le orecchie, si presenta con dolore, gonfiore, arrossamento e prurito dovuti alla crescita del fungo sui detriti di cerume che si trovano nell’orecchio esterno. La terza riguarda le unghie dei piedi ed è contraddistinta soprattutto da fragilità ungueale e deformazione dolorosa (dovuta a detriti al di sotto delle unghie), anche se in alcune circostanze la superficie dell’unghia può diventare bianca e polverulenta. Nella quarta troviamo soprattutto congiuntiviti, i cui sintomi sono rossore, fotofobia, bruciore, secrezione purulenta e aumento della lacrimazione, ed endoftalmiti (rare), che si manifestano con iperemia congiuntivale, dolore intenso, abbassamento della vista ed edema palpebrale. Per quanto concerne l’ultima, si sviluppa specialmente nelle persone con piaghe da decubito e/o ustioni e paraplegiche, i cui sintomi sono simili a quelli della dermatomicosi o tigna (infezione da funghi dermatofiti come Trichophyton, Epidermophyton e Microsporum);
- Aspergillosi invasiva, specifica dei pazienti immunodepressi, è la forma più dannosa e letale. In questa tipologia di aspergillosi le ife fungine, dopo essersi formate a livello dei polmoni, invadono il torrente ematico provocando trombi, infarti ed emorragie, e si possono diffondere ai diversi organi. A seconda dell’organo colpito si discernono quattro forme cliniche: disseminata (che implica il cervello, la cute, i reni, gli occhi e il cuore), polmonare, rino-sinusale e tracheo-bronchiale.
Metodi di identificazione
Nel momento in cui si sospetta un caso di aspergillosi, la diagnosi inizia con l’esecuzione di esami come la radiografia del torace (Fig. 5A) e la tomografia computerizzata (TC). Se si notano degli indici singolari della malattia, l’indagine prosegue con l’isolamento del fungo da campioni come essudato pleurico, secrezioni bronchiali, espettorato, lavaggio bronco-alveolare e prelievi mediante broncoscopia. È opportuno sottolineare che l’espettorato può fornire dei falsi positivi, in quanto l’Aspergillus può risiedere nel cavo orale come commensale.
Una volta prelevato il campione, si esegue l’analisi al microscopio che consente di rimarcare i conidi scuri dai margini irregolari e i conidiofori marroni (Fig. 5B). Insieme a questo esame si ricorre anche all’indagine colturale su agar Sabouraud Destrosio, PDA, CYA e MEA.

Nel caso dell’aspergillosi broncopolmonare allergica si eseguono il dosaggio delle IgE specifiche anti-Aspergillus mediante il RAST (saggio di radioallergoassorbimento) e la conta degli eosinofili nel sangue.
Quando è necessario identificare e differenziare il micete da altri funghi, si impiega il sequenziamento genomico. Nel caso in cui bisogna individuare e quantificare le ocratossine, la metodica da usare è la cromatografia su strato sottile (Fig. 6).

Trattamento e prevenzione
Le forme leggere dell’aspergillosi si possono curare con facilità; i farmaci maggiormente impiegati sono gli antimicotici come il Voriconazolo, il Posaconazolo, l’Itraconazolo, l’Amfotericina B e la Caspofungina. Il primo, il secondo e il terzo interferiscono con l’azione di enzimi essenziali per la sintesi dell’ergosterolo (come la 14α-demetilasi), uno sterolo che raffigura un componente importante delle membrane cellulari dei miceti. Il quarto si infiltra nella membrana plasmatica e ne deteriora la permeabilità, con conseguente perdita di ioni e molecole organiche. Contrariamente ai precedenti, l’ultimo non agisce sulla membrana, bensì sulla parete cellulare; impedisce la formazione della parete cellulare mediante l’inibizione dell’enzima glucano sintetasi, che serve per la genesi del polisaccaride 1,3-β-glucano, costituente della parete cellulare.
Se ci troviamo di fronte ad aspergillosi broncopolmonare allergica, è utile associare anche i corticosteroidi al fine di attenuare l’infiammazione.
Per l’otomicosi, l’utilizzo di Itraconazolo e antiinfiammatori non steroidei (tachipirina, aspirina) permette di alleviare il dolore.
Considerando che le aspergillosi invasive di frequente hanno una prognosi sfavorevole, anche se si ha solamente il sospetto di aspergillosi, è comunque consigliato rivolgersi a un medico.
La profilassi dell’aspergillosi consiste nella rimozione delle spore di A. niger e nel blocco della crescita mediante un trattamento chimico e antifungino con 70% di etanolo o alcol isopropilico per dieci minuti, che è efficace per uccidere le spore che penetrano nei muri e le eventuali ife.
Per prevenire l’otomicosi, è necessario evitare di fare entrare acqua nelle orecchie quando si nuota (oppure applicare gocce all’acido acetico dopo l’entrata dell’acqua nelle orecchie), asciugare le orecchie dopo la doccia, non utilizzare i tamponi di cotone e non grattare la pelle fuori e dentro le orecchie.
Approcci biotecnologici
A. niger è conosciuto per il suo impiego in ambito industriale per la produzione di acido citrico (o citrato), acido gluconico e svariati enzimi tra cui glucoamilasi, pectinasi, α-galattosidasi, glucosio ossidasi e glicoside idrolasi. Quest’ultimo è usato per convertire la biomassa in biocarburante disintegrando la cellulosa e l’emicellulosa contenute nelle pareti cellulari delle piante; questi due polisaccaridi vengono quindi trasformati in una sostanza che può essere convertita in etanolo.
A proposito della sintesi di acido citrico, già nel 1917 il chimico James Currie scoprì che oggi ceppo di A. niger era in grado di sintetizzare questo acido tricarbossilico quando cresceva in un mezzo zuccheroso (ricordiamo che l’acido citrico raffigura un intermediario del ciclo di Krebs, una tappa del processo di ossidazione del glucosio o degli acidi grassi); inoltre, riusciva a proliferare a pH molto acido (2,5-3,5). Due anni dopo la scoperta di Currie, iniziò la produzione a livello industriale utilizzando A. niger, la fermentazione chimica prosperò e nacque la biotecnologia industriale. Un secolo dopo la generazione di acido citrico mediante questo micete diventò un settore che fruttava bilioni di dollari. Nel 2007 si reputava una produzione mondiale di 1,6 milioni di tonnellate, con un valore stimato di 2,6 bilioni di dollari nel 2014 e un incremento previsto a 3,6 bilioni nel 2020. Poiché si tratta di un acido debole, si può impiegare come antiossidante, conservante, acidificante, regolatore di pH o per insaporire cibi e bevande.
Generalmente la fabbricazione di acido citrico richiede una crescita della muffa in ambiente aerobio e in soluzione zuccherosa, che di solito proviene da risorse economiche come la melassa, il liquore ripido di granoturco o l’idrolisato di amido di mais. Dopo la fermentazione, A. niger viene fisicamente rimosso, normalmente tramite filtrazione, e l’acido citrico è estratto mediante precipitazione della miscela di fermentazione con idrossido di calcio, allo scopo di creare il sale di citrato di calcio. In seguito al trattamento con acido solforico, si giunge alla realizzazione del citrato.
Comunque, l’utilizzazione di A. niger non si limita alla fabbricazione dell’acido citrico, bensì viene usato come “industria cellulare” data la sua capacità di generare una certa gamma di enzimi, come ad esempio le proteasi, che trovano applicazione in ambito farmaceutico e cosmetico (per l’eliminazione della cheratina nell’acne o nella psoriasi, per la rimozione dei calli, per la depilazione, per la rigenerazione degli epiteli e per accelerare i processi di guarigione), nei detergenti da bucato (per incrementare la capacità smacchiante e per renderli più sicuri dal punto di vista ambientale) e nel settore alimentare (per il miglioramento della digeribilità e della qualità sensoriale dei cibi, come anche nella riduzione dei componenti allergenici). È chiaro in questi ambiti non sono utilizzate solo le proteasi di A. niger, ma anche di altre specie (A. fumigatus, A. flavus, A. clavatus, A. oryzae) e di altri funghi (Penicillium spp., Botrytis cinerea, Conidiobolus coronatus).
In aggiunta a ciò, A. niger è adatto per la produzione di una vasta quantità di frutto-oligosaccaridi (sostanze ad azione prebiotica per la flora intestinale) grazie all’espressione di enzimi che scindono gli zuccheri complessi (pectinasi, glucoamilasi).
Infine, A. niger possiede una grande capacità di bioassorbimento, e per tale ragione le sue colonie si impiegano allo scopo di aumentare l’assorbimento di alcune sostanze coloranti come il Rosso Congo e il Blu brillante FCF, e la rimozione delle loro impurità.
Fonti
- M. Abarca, M. Bragulat, G. Castellá e F. Cabañes. 1994. “Ochratoxin A production by strains of Aspergillus niger var. niger”, Appl Environ Microbiol
- E. Schuster, N. Dunn-Coleman, J.C. Frisvad e P.W. van Dijck. 2002. “On the safety of Aspergillus niger—a review”, Applied Microbiology and Biotechnology
- D.G. Jone. 2013. “The Epidemiology of Plant Diseases”, Springer
- Marta Cortesão, Aram de Haas, Rebecca Unterbusch, Akira Fujimori, Tabea Schütze, Vera Meyer and Ralf Moeller. 2020. “Aspergillus niger Spores Are Highly Resistant to Space Radiation”, Frontiers in Microbiology
- R. Cevenini e V. Sambri, 2004. “Microbiologia e microbiologia clinica”, Piccin
- Paula Monteiro de Souza, Mona Lisa de Assis Bittencourt, Carolina Canielles Caprara, Marcela de Freitas, Renata Paula Coppini de Almeida, Dâmaris Silveira, Yris Maria Fonseca, Edivaldo Ximenes Ferreira, Filho, Adalberto Pessoa, Junior and Pérola Oliveira Magalhães. 2015. “A biotechnology perspective of fungal proteases”, Braz J Microbiol
- Timothy C. Cairns , Corrado Nai, Vera Meyer. 2018. “How a fungus shapes biotechnology: 100 years of Aspergillus niger research”, Fungal Biol Biotechnol
- L.G.A. Ong, S. Abd-Aziz, S. Noraini, M.I.A. Karim e M. A. Hassan. 2004. “Enzyme Production and Profile by Aspergillus niger During Solid Substrate Fermentation Using Palm Kernel Cake as Substrate”, Applied Biochemistry and Biotechnology
- https://www.syngenta.nl/it/seedcare/vegetables/diseases/aspergillus/aspergillus-niger
- https://www.my-personaltrainer.it/benessere/aspergillus.html
- http://www.informazionisuifarmaci.it/onicomicosi-quale-trattamento
- https://it.qaz.wiki/wiki/Aspergillus_niger
- https://www.chaetomiumqueen.com/aspergillus-niger/
- https://it.ilovevaquero.com/zdorove/114042-aspergillus-niger-chto-eto-morfologiya-lechenie.html
- https://microbenotes.com
- https://www.msdmanuals.com/it-it/professionale/disturbi-oculari/uveite-e-disturbi-correlati/endoftalmite
- https://www.humanitas.it/malattie/congiuntivite
- https://www.torrinomedica.it/schede-farmaci/voriconazolo_sandoz_gmbh_200_mg_polv_sol_inf_1_fl_/
- https://www.humanitas.it/enciclopedia/principi-attivi/antifungini/posaconazolo
- https://www.my-personaltrainer.it/farmaci/cancidas.html
- https://www.my-personaltrainer.it/salute-benessere/itraconazolo.html
- https://www.my-personaltrainer.it/salute-benessere/amfotericina-B.html
- https://docplayer.it/56598733-Tecniche-di-purificazione-cromatografia.html
- https://www.msdmanuals.com/it-it/professionale/malattie-polmonari/asma-e-disturbi-correlati/aspergillosi-broncopolmonare-allergica
- https://www.pathologyoutlines.com/topic/lungnontumoraspergillosis.html
Salve avrei bisogno di una vostra opinione, è cresciuta una strana muffa nella cuccia del cane e sono molto curiosa cosa è….mi sembra una specie aliena 😂
Salve Daniela. Ci mandi pure delle foto di questa muffa, così riusciamo a capire di che specie si tratta