Un gruppo di giovani ricercatori di Pisa ha creato un sensore grafenico per monitorare i biofilm di Escherichia coli, Pseudomonas aeruginosa e Staphylococcus aureus
Cos’è un sensore?
Un sensore chimico è un sistema in grado di trasformare un’informazione chimica in un segnale misurabile analiticamente utile. L’informazione chimica spazia dalla concentrazione di un singolo componente specifico alla concentrazione di tutti i componenti presenti nel campione analizzato.
Un sensore è un dispositivo che utilizza un elemento di riconoscimento mantenuto a contatto diretto con un trasduttore. In particolare, ogni sensore è solitamente costituito da tre parti (Fig. 1):
- un recettore selettivo per uno specifico analita target;
- un trasduttore, solitamente fisico-chimico, ottico, piezoelettrico, elettrochimico, ecc., che trasforma il segnale risultante dall’interazione dell’analita con il recettore in un segnale misurabile e quantificabile;
- una componente elettronica di amplificazione ed elaborazione del segnale, che permette di ottenere risultati facilmente interpretabili.

L’importanza moderna dei sensori
Lo sviluppo di sensori chimici sembra destinato a rivoluzionare le potenzialità nel campo della chimica analitica. Le metodologie analitiche classiche richiedono il prelievo, il trasporto e, in molti casi, un trattamento del campione. Inoltre, esse richiedono spesso strumentazioni costose utilizzabili solo da personale altamente specializzato.
Per cui, in passato, la caratterizzazione di un sistema da un punto di vista chimico veniva fortemente condizionata da una serie di fattori pratici, la maggior parte dei quali correlata a questioni di tempo e di costo, che spesso rendevano questo tipo di analisi non implementabili.
La chimica dei sensori nasce come soluzione a queste restrizioni e ricopre un largo campo di applicazione dove le strategie convenzionali, anche quando flessibili, risultano inadeguate. Inoltre, i sensori chimici sono di particolare interesse in quanto, non solo sono economici e facili da utilizzare, ma anche perché, se propriamente progettati, possono permettere il monitoraggio delle concentrazioni di un analita in tempo e talvolta in spazio reale.
È evidente, però, come lo studio e la progettazione di sensori chimici ad alta efficienza richieda un approccio multidisciplinare. È infatti essenziale la cooperazione di chimici, fisici, biologi ed ingegneri.
Perché è importante monitorare la formazione di biofilm batterici?
Si definisce biofilm l’insieme di cellule batteriche adese e inglobate in una matrice polisaccaridica adesiva secreta dalle cellule stesse (Fig. 2).
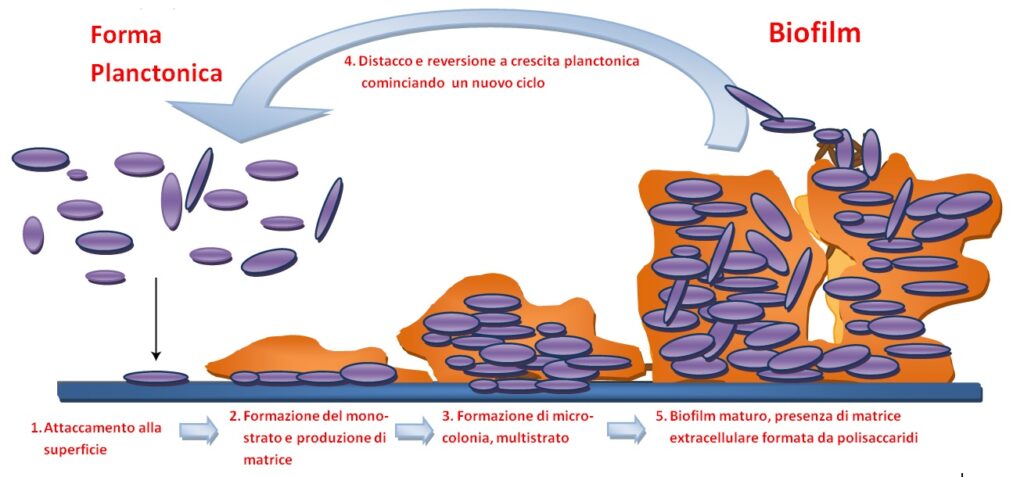
Il biofilm assolve a diverse funzioni tra cui quella di difesa da dilavamento, fagocitosi e antibiotici; quella di nicchia per l’accumulo di nutrienti; quella di scambio di materiale genico e non; ed infine quella di favoreggiamento della crescita soprattutto negli ambienti naturali.
Il controllo della formazione di biofilm batterici è di fondamentale importanza sia nel settore sanitario, per la cura di patologie (fibrosi cistica, tubercolosi, ecc.), per il miglioramento degli antibiotici, per la sicurezza di dispositivi medici e protesi (es. cateteri, placche dentali), sia nel settore industriale, per impedire l’ostruzione e il deterioramento delle condutture degli impianti (es. acquedotti).
In particolare, la formazione di biofilm batterici su dispositivi medici (Fig. 3) e tessuti rappresenta una problematica di primaria importanza in quanto i biofilm sono responsabili di circa l’80% delle infezioni microbiche umane.

Le infezioni associate a biofilm sono difficili da curare e i pazienti sono spesso soggetti a ricadute in quanto i microrganismi all’interno di un biofilm presentano una suscettibilità altamente ridotta al sistema immunitario dell’ospite e agli antibiotici.
Attualmente, il rilevamento di un biofilm può essere effettuato utilizzando tecniche basate sulla crescita mediante coltura, approcci molecolari e microscopia. Tuttavia, essi richiedono molto tempo, personale specializzato e, cosa più importante, non sono in grado di monitorare lo sviluppo del biofilm in vivo. Di conseguenza, spesso è necessaria una biopsia nei pazienti o l’asportazione del dispositivo compromesso dalla contaminazione microbica.
Il sensore italiano per il monitoraggio dei biofilm
Il lavoro di ricerca di un gruppo di giovani ricercatori italiani dell’Università di Pisa, guidati dal Prof. Fabio Di Francesco, si è incentrato sullo sviluppo di un innovativo sensore in grado di monitorare la formazione di un biofilm in tempo reale.
Il recente studio scientifico dal titolo “A graphenic and potentiometric sensor for monitoring the growth of bacterial biofilms” ha avuto come obiettivo lo sviluppo di un sensore grafenico flessibile a basso costo (Fig. 4) che consente un monitoraggio in tempo reale della crescita di due comuni batteri Gram-negativi, quali Escherichia coli e Pseudomonas aeruginosa, e di una specie batterica Gram-positiva, quale Staphylococcus aureus. Tali specie sono state selezionate in quanto sono note per essere responsabili dello sviluppo di infezioni associate al biofilm.

Secondo gli autori di questo studio: “La tecnica di trasduzione utilizzata, Open Circuit Potential (OCP), ha rilevato in modo efficiente la crescita del biofilm localizzata sulla superficie del sensore in terreni di coltura liquidi e semisolidi, mostrando una correlazione negativa significativa rispetto alla crescita batterica” (Fig. 5).

Inoltre, i giovani autori, attualmente dottorandi di ricerca in Scienze Chimiche e dei Materiali presso il Dipartimento di Chimica e Chimica Industriale, hanno spiegato che: “I biofilm sono di natura complessa, per cui l’interazione di una varietà di fattori sulla superficie dell’elettrodo può determinare la variazione dell’OCP nel tempo. È stato ipotizzato che processi come l’accumulo di una carica negativa netta, il metabolismo batterico e la respirazione cellulare possano spiegare la diminuzione dell’OCP”.
I vantaggi della scoperta
Secondo i ricercatori: “Questa idea nasce dall’esigenza di provare a prevenire, controllare e curare le infezioni associate a biofilm batterici. La flessibilità della scheda di rilevamento rende questo sensore adatto ad applicazioni complesse legate alla salute umana, come ad esempio il monitoraggio dello sviluppo del biofilm nei dispositivi medici (es. lume dei cateteri) e nelle ferite croniche”.
Lo sviluppo di questa tipologia di sensori chimici, insieme ai sempre più studiati biosensori, rappresenterà un supporto fondamentale per la medicina personalizzata del futuro, con un notevole risparmio di costi e tempi ma soprattutto con un significativo beneficio per la vita dei pazienti che potranno evitare, in molti casi, delle biopsie invasive.
Nicola Di Fidio
Sitografia:
- Nicola Di Fidio (11 ottobre 2017, Microbiologia Italia). Anche i batteri parlano tra loro attraverso il quorum sensing. Estrapolato da: https://www.microbiologiaitalia.it/batteriologia/anche-i-batteri-parlano-tra-loro-attraverso-il-quorum-sensing/
- Nicola Di Fidio (17 giugno 2020, Microbiologia Italia). Un innovativo biosensore per il monitoraggio in tempo reale dell’urea durante la dialisi. Estrapolato da: https://www.microbiologiaitalia.it/batteriologia/un-innovativo-biosensore-per-il-monitoraggio-in-tempo-reale-dellurea-durante-la-dialisi/
- Nicola Di Fidio (6 giugno 2018, Microbiologia Italia). Diagnosi via app grazie ad un biosensore ingeribile contenente batteri. Estrapolato da: https://www.microbiologiaitalia.it/batteriologia/diagnosi-via-app-grazie-ad-un-biosensore-ingeribile-contenente-batteri/
- Alice Marcantonio (24 giugno 2018, Microbiologia Italia). Un sistema batterico-elettronico ingeribile monitora la salute gastrointestinale. Estrapolato da: https://www.microbiologiaitalia.it/batteriologia/un-sistema-batterico-elettronico-ingeribile-monitora-la-salute-gastrointestinale/
- Maria Laura Luprano (8 ottobre 2016, Microbiologia Italia). In arrivo un nano-fiore portatile capace di rilevare anche quantità minime di patogeni alimentari. Estrapolato da: https://www.microbiologiaitalia.it/batteriologia/arrivo-un-nano-fiore-portatile-capace-rilevare-anche-quantita-minime-patogeni-alimentari/
Bibliografia:
- Poma, N., Vivaldi, F., Bonini, A., Salvo, P., Kirchhain, A., Melai, B., Battai, D., Tavanti, A., Di Francesco, F. (2020). A graphenic and potentiometric sensor for monitoring the growth of bacterial biofilms. Sensors and Actuators B: Chemical, 128662.
- Miller, M. B., & Bassler, B. L. (2001). Quorum sensing in bacteria. Annual Reviews in Microbiology, 55(1), 165-199.
- Bassler, B. L. (2002). Small talk: cell-to-cell communication in bacteria. Cell, 109(4), 421-424.
Crediti immagini:
- https://www.labmanager.com/news/crumpled-graphene-makes-ultra-sensitive-cancer-dna-detector-22110
- https://docplayer.it/8426352-Sensori-chemical-chemical.html
- Poma, N., Vivaldi, F., Bonini, A., Salvo, P., Kirchhain, A., Melai, B., Battai, D., Tavanti, A., Di Francesco, F. (2020). A graphenic and potentiometric sensor for monitoring the growth of bacterial biofilms. Sensors and Actuators B: Chemical, 128662.
- https://simsi.it/oblo-sul-wound-care-di-klarida-hoxha/il-microbioma-di-una-lesione-cutanea-come-rompere-lequilibrio-batterico/
- https://www.meddeviceonline.com/doc/reducing-biofilm-buildup-on-implanted-devices-with-liquid-infused-polymers-0001